Kaliumvätekarbonat
| Kaliumbikarbonat | |
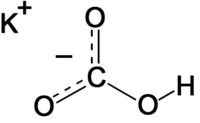 | |
| Systematiskt namn | Kaliumvätekarbonat |
|---|---|
| Övriga namn | Kaliumbikarbonat |
| Kemisk formel | KHCO3 |
| Molmassa | 100,1151 g/mol |
| Utseende | Vita eller färglösa kristaller |
| CAS-nummer | 298-14-6 |
| SMILES | OC(=O)[O-].[K+] |
| Egenskaper | |
| Densitet | 2,17 g/cm³ |
| Löslighet (vatten) | 322 g/l |
| Smältpunkt | 100 – 120 °C (sönderfaller) |
| Faror | |
| NFPA 704 | |
| LD50 | 2064 mg/kg |
| SI-enheter & STP används om ej annat angivits | |
Kaliumvätekarbonat eller kaliumbikarbonat är ett salt av kalium och kolsyra med formeln KHCO3.
Egenskaper[redigera | redigera wikitext]
Kaliumvätekarbonat är lösligt i vatten, men inte i etanol. Vattenlösningens pH blir ca 8,6.[1] När kaliumvätekarbonat värms upp över 100 °C sönderfaller det till kaliumkarbonat (K2CO3), vatten och koldioxid.
Framställning[redigera | redigera wikitext]
Kaliumvätekarbonat framställs genom att låta kaliumkarbonat reagera med koldioxid och vatten.
- K2CO3 + CO2 + H2O → 2 KHCO3
Visserligen bildas liten del (någon procent) vätekarbonatjoner när kaliumkarbonat löses i vatten.
- 2K+ HCO3- + OH-
men detta är ingen framställningsmetod. Om vattnet dunstar återbildas kaliumkarbonat.
Användning[redigera | redigera wikitext]
Kaliumbikarbonat används huvudsakligen som en källa till koldioxid i till exempel bakpulver och i pulversläckare.
Det används också som surhetsreglerande medel i till exempel bordsvatten.
Kaliumbikarbonat används också inom jordbruk som ett miljövänligt bekämpningsmedel mot mjöldagg.
Se även[redigera | redigera wikitext]
Källor[redigera | redigera wikitext]
- ^ [1] Arkiverad 31 augusti 2019 hämtat från the Wayback Machine. data om kaliumvätekarbonat i den tyska dabasen GESTIS, läst 2018-10-14
- Material Safety Data Sheet Mallinckrodt Baker
- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Potassium bicarbonate, tidigare version.
- Den här artikeln är helt eller delvis baserad på material från tyskspråkiga Wikipedia, Kaliumhydrogencarbonat, tidigare version.



