Natriumtiosulfat
| Natriumtiosulfat | |
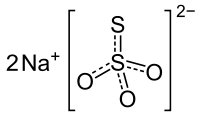  | |
| Systematiskt namn | Natriumtiosulfat |
|---|---|
| Övriga namn | Hyposulfitsoda, hypo |
| Kemisk formel | Na2S2O3 |
| Molmassa | 158,108 g/mol |
| Utseende | Vita kristaller |
| CAS-nummer | 7772-98-7 |
| SMILES | [O-]S(=S)(=O)[O-].[Na+].[Na+] |
| Egenskaper | |
| Densitet | 1,667 g/cm³ |
| Löslighet (vatten) | 209 g/l (20 °C) |
| Smältpunkt | 48,3 °C |
| Kokpunkt | 100 °C (sönderfaller) |
| Faror | |
| NFPA 704 | |
| SI-enheter & STP används om ej annat angivits | |
Natriumtiosulfat är ett tiosulfatsalt av natrium.
Framställning[redigera | redigera wikitext]
Industriellt produceras natriumtiosulfat som en biprodukt vid tillverkningen av natriumsulfid. För laboratoriebruk kan saltet framställas genom att värma upp natriumsulfit tillsammans med svavel.
Egenskaper[redigera | redigera wikitext]
Natriumtiosulfat kan neutralisera hypoklorit vilket är den aktiva ingrediensen i klorbaserade blekmedel.
Det kan också reagera med guld och bilda molekylen Na3[Au(S2O3)2].
Användning[redigera | redigera wikitext]
- Natriumtiosulfat kan användas som ett alternativ till natriumcyanid vid utvinning av guld. Nackdelen är att guldtiosulfat-jonerna inte kan filtreras fram med aktivt kol.
- Som fixerbad vid fotografisk framkallning. Ämnet går inom fotobranschen under namnet Hyposulfitsoda eller Hypo.
- För att kunna testa pH-värdet på blekmedel. Natriumtiosulfat neutraliserar hypoklorit-joner som annars skulle ha blekt bort färgerna av pH-indikatorn.
- Underkylt natriumtiosulfat kristalliserar sig med en exoterm reaktion vilket gör den användbar i till exempel kemiska handvärmare.
- Som motgift till cyanid. Natriumtiosulfat överför svavel-atomer till cyanid som övergår i ofarlig tiocyanat.
- Vid garvning av läder.
- För att neutralisera det jod-baserade konserveringsmedlet Lugols lösning. Lösningen konserverar till exempel celler i växtplanktonprover bruna, men tillsätter men natriumtiosulfat avfärgas provet och nya färgämnen kan tillsättas.



