Fosfin
| Fosfin | |
  | |
| Systematiskt namn | Fosfan |
|---|---|
| Övriga namn | Fosfamin, Fosfortrihydrid, Fosforerat väte, vätefosfid |
| Kemisk formel | PH3 |
| Molmassa | 33,9976 g/mol |
| Utseende | Färglös gas |
| CAS-nummer | 7803-51-2 |
| SMILES | P |
| Egenskaper | |
| Densitet | 1,379 g/cm³ |
| Löslighet (vatten) | 321 g/l (17 °C) |
| Smältpunkt | -132,8 °C |
| Kokpunkt | -87,7 °C |
| Faror | |
| Huvudfara | |
| NFPA 704 | |
| SI-enheter & STP används om ej annat angivits | |
Fosfin (vars systematiska namn är fosfan) är en mycket giftig och brandfarlig gasformig fosforförening med den kemiska formeln PH3. Ren fosfingas är luktlös, men oftast är den förorenad av difosfin (P2H4), ett ämne som har en obehaglig lukt av fisk och vitlök.
Fosfin bildas först vid extrem anoxi och mycket låga pE-värden, då fosfat-fosfor kan reduceras till fosfin.
Fosfin ska inte förväxlas med fosgen, som också är giftig.
Fosfiner
En klass som är relaterad till PH3 är de fosfororganiska föreningarna vanligtvis kallade "fosfiner." Dessa alkyl- och arylderivat av fosfin är analoga till aminer. Vanliga exempel inkluderar trifenylfosfin ((C6H5)3P) och BINAP; båda används som ligander i homogen katalys. Fosfiner oxideras lätt till fosfinoxider vilket exemplifieras genom direkt syntes av en fosfakrona, fosforanalogen till en azakrona, där det inte är möjligt att isolera själva fosfinmolekylerna.

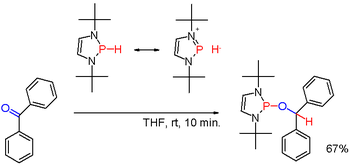
Väl modifierad med lämpliga substituenter som i vissa (ovanliga) diazafosfolener (reaktionsschema 3) kan polariteten av P-H-bindningen inverteras och den resulterande fosfinhydriden kan reducera en karbonylgrupp som i exemplet med bensofenon på ytterligare ett sätt.
Se även
Ämnen
Grupper
- Fosfinoxid, R3PO
- Fosforan, R3PR2
- Fosfinit, R2(RO)P
- Fosfonit, R(RO)2P
- Fosfit, (RO)3P
- Fosfinat, R2P(RO)O
- Fosfonat, RP(RO)2O
- Fosfat, P(RO)3O
Referenser
- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Phosphine, 17 april 2010.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

