Fosfit
| Den här artikeln behöver källhänvisningar för att kunna verifieras. (2020-03) Åtgärda genom att lägga till pålitliga källor (gärna som fotnoter). Uppgifter utan källhänvisning kan ifrågasättas och tas bort utan att det behöver diskuteras på diskussionssidan. |

|
|
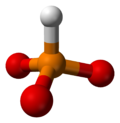
| Fosfitjon (HPO32– ) | |
|---|---|
Fosfiter är salter och estrar av fosforsyrlighet (H3PO3). Fosfitjonen består av en fosforatom omgiven av tre syreatomer och en väteatom som bildar en tetraeder. Fosforatomen befinner sig i oxidationstillstånd +3 och hela jonen har laddningen -2.
Fosfit är korresponderande bas till fosforsyrlighet.
Resonans[redigera | redigera wikitext]
Fosfitjonen stabiliseras genom resonans där de två överskottselektronerna delas mellan de tre syreatomerna.
Varianter[redigera | redigera wikitext]
Vätefosfit[redigera | redigera wikitext]
Delvis dissocierad fosforsyrlighet bildar vätefosfit-joner (H2PO3–). Kallas även för bifosfit eller sur fosfit.
Pyrofosfit[redigera | redigera wikitext]
Genom att värma fosfit under lågt tryck kan man framställa pyrofosfit-joner (H2P2O52–).
Salter[redigera | redigera wikitext]
Fosfitsalter som kaliumvätefosfit (KH2PO3) och natriumfosfit (Na2HPO3) är lättlösliga i vatten.
Estrar[redigera | redigera wikitext]
 |
Fosfitestrar är organiska föreningar med tre kolvätekedjor bundna till fosfitens tre syreatomer. De brukar vanligen framställas genom att reagera alkohol med fosfortriklorid (PCl3) i stället för fosforsyrlighet.
Se även[redigera | redigera wikitext]
Ämnen[redigera | redigera wikitext]
- Fosforsyrlighet - H3PO3
Grupper[redigera | redigera wikitext]
- Fosfin - PR3
- Fosfinoxid - OPR3
- Fosfinit - P(OR)R2
- Fosfonit - P(OR)2R
- Fosfinat - OP(OR)R2
- Fosfonat - OP(OR)2R
- Fosfat - OP(OR)3
- Fosforan - R3PR2
Referenser[redigera | redigera wikitext]
- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Phosphite, 23 januari 2010.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||


