Kaliumcyanid
| Kaliumcyanid | |
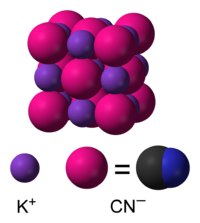 | |
| Systematiskt namn | Kaliumcyanid |
|---|---|
| Övriga namn | Cyankalium |
| Kemisk formel | KCN |
| Molmassa | 65,1 g/mol |
| Utseende | Färglösa kristaller med arom av bittermandel |
| CAS-nummer | 151-50-8 |
| SMILES | [N#C-].[K+] |
| Egenskaper | |
| Densitet | 1,560 g/cm³ |
| Löslighet (vatten) | 716 g/l (25 °C) |
| Smältpunkt | 634,5 °C |
| Kokpunkt | 1625 °C |
| Faror | |
| Huvudfara | |
| NFPA 704 | |
| LD50 | 5 mg/kg |
| SI-enheter & STP används om ej annat angivits | |
Kaliumcyanid (KCN), även cyankalium, är kaliumsaltet av syran vätecyanid (HCN). Ämnet har varit vanligt som gift samt vid utvinning av guld.
Egenskaper

Kaliumcyanid bildar kristaller med bittermandelarom. Ämnet uppvisar god löslighet i vatten, men inte i alkohol. Endast i genomsnitt varannan människa kan förnimma den dödliga bittermandellukten.
Framställning
Kaliumcyanid framställs normalt genom att leda vätecyanidgas genom en lösning med kalilut.
Förr tillverkades kaliumcyanid genom att kolmonoxid och ammoniak tillfördes kaliumkarbonat (K2CO3) vid en temperatur om 600 °C.
Användning
Kaliumcyanid används huvudsakligen vid giftmord men även vid utvinning av guld och i galvaniska bad. Cyankalium användes även vid behandling av fotografiska glasplåtar
Toxikologi
Cyankalium i sig är inte farligt men när ämnet når magsäcken metaboliseras ämnet på ungefär 20 minuter till cyanväte[1]. Cyanväte är ett giftigt ämnet som inaktiverar cellandningen genom att binda till järnet i proteinet cytokrom C som är vitalt för mitokondriernas överlevnad.
Säkerhet
Inandning av ånga eller rök innehållande kaliumcyanid kan vara livsfarlig, och vid handhavande av ämnet måste skyddsmask bäras. Vidare måste vid handhavande gummihandskar bäras, då ämnet kan tränga igenom huden.



