Fosfoanhydridbindning
Fosfoanhydridbindningar är energirika anhydridbindningar mellan fosfatgrupper.[1] De förekommer exempelvis i ATP, som används vid energikrävande kemiska processer i kroppens celler.[1]
Fosfoanhydridbindningar skapas genom derivatisation och dehydratisation av fosforsyra. Hydrolys av dessa bindningar blir därför exergon.
Exemplet ATP[redigera | redigera wikitext]
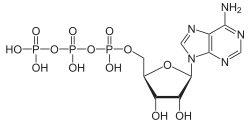
Fosfatgrupperna benämns alfa, beta och gamma i ordning från ribosgruppen och ut.
I adenosintrifosfat (ATP) finns det två stycken fosfoanhydridbindningar. Dessa binder ihop gammafosfatgruppen och betafosfatgruppen, respektive betafosfatgruppen och alfafosfatgruppen. Därför har dissociation av ATP genom hydrolys till adenosindifosfat (ADP) eller adenosinmonofosfat (AMP) ett negativt energiutbyte.[2]
Hydrolys av fosfoanhydridbindningen mellan gammafosfatgruppen och betafosfatgruppen ger ett negativt energiutbyte på -30,5 kJ/mol (räknat i Gibbs fria energi):
- ATP+H2O→ADP+Pi
- ΔG´°=-30,5 kJ/mol
Hydrolys av fosfoanhydridbindningen mellan betafosfatgruppen och alfafosfatgruppen ger i sin tur ett negativt energiutbyte på -45,6 kJ/mol (räknat i Gibbs fria energi):
- ATP+H2O→AMP+PPi
- ΔG´°=-45,6 kJ/mol
Beteckning[redigera | redigera wikitext]

En fosfoanhydridbindning markeras ofta på detta sätt: ~. ATP skulle därför kunna skrivas A-P~P~P och ADP A-P~P. Denna markering är uppfunnen av den tysk-amerikanska biokemisten Fritz Albert Lipmann, som också upptäckte koenzym A och forskade på dess roll inom metabolismen.
Se även[redigera | redigera wikitext]
Referenser[redigera | redigera wikitext]
- ^ [a b] Thomas M. Devlin (red.) (1992): Textbook of Biochemistry. With Clinical Correlations. Third edition. Wiley-Liss. ISBN 0-471-51348-2.
- ^ Campbell, Neil A. (1993). Biology. Third edition. Benjamin-Cummings Pub Co
