Koenzym
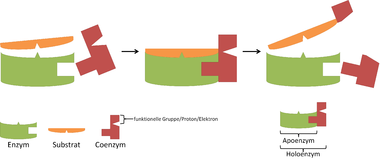
Ett koenzym är en organisk molekyl som binder till ett enzym för att bidra till dess katalytiska förmåga.[1] Det funktionellt inaktiva enzymet bestående av enbart protein kallas apoenzym, medan den aktiva formen med bundet koenzym (och möjligen andra kofaktorer) kallas holoenzym.
Koenzymer är dissocierbara (mindre hårt bundna) organiska ämnen av relativt låg molekylmassa och överför kemiska grupper, vätejoner eller elektroner i samband med den enzymatiska reaktionen.[1] Kemiskt är koenzymer ofta nukleotider, och är till skillnad från apoenzymet inte proteiner. Eftersom koenzymet förändras kemiskt i de reaktioner som enzymet katalyserar måste det därför ändras tillbaka till ursprungsformen av ett annat enzym.
Koenzymer är en del av den bredare ämnesgruppen kofaktorer, som även inkluderar andra kemiska föreningar, såsom metalljoner och prostetiska grupper, som är hårdare bundna till enzymet.[2]
Exempel på koenzymer är nikotinamidadenindinukleotid (NAD), som accepterar vätejoner, och adenosintrifosfat (ATP), som lämnar från sig fosfatgrupper samtidigt som de överför kemisk energi.[3] De flesta B-vitaminer är också koenzymer.
