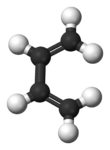
Butadien
| Butadien | |
  | |
| Systematiskt namn | 1,3-butadien |
|---|---|
| Kemisk formel | C4H6 |
| Molmassa | 54,09 g/mol |
| Utseende | Färglös gas |
| CAS-nummer | 106-99-0 |
| SMILES | C=CC=C |
| Egenskaper | |
| Löslighet (vatten) | 1 g/l |
| Smältpunkt | -108,9 °C |
| Kokpunkt | -4,4 °C |
| Faror | |
| Huvudfara | |
| NFPA 704 | |
| SI-enheter & STP används om ej annat angivits | |
Butadien, egentligen 1,3-butadien, är en enkel konjugerad dien. Butadien kan också syfta på isomeren 1,2-butadien, men den är svår att framställa och saknar industriell betydelse.
Framställning[redigera | redigera wikitext]
Den huvudsakliga framställningsmetoden är genom krackning av aromatiska kolväten. När de hettas upp till cirka 900 °C går de sönder och bildar omättade kolväten som butadien, etylen och acetylen. De olika alkenerna separeras sedan från varandra genom destillation.
Det går också att framställa butadien genom att låta etanol (C2H5OH) och acetaldehyd (C2H4O) reagera med tantal som katalysator.
Den senare metoden var vanlig i Sovjetunionen under och strax efter andra världskriget och används fortfarande i Kina och Indien.
Struktur[redigera | redigera wikitext]
Rotation runt den centrala bindningen i butadien ger upphov till olika konformationer. Den stabilaste konformationen är s-trans-formen, där dubbelbindningarna är riktade bort från varandra. Två andra, "skeva" konformationer, där dubbelbindningarna är riktade åt nästan samma håll, är också lokala energiminima. Den konformation där dubbelbindningarna är riktade åt samma håll kallas s-cis-formen, och är ett övergångstillstånd (ett energimaximum) mellan de båda skeva konformationerna.[1]
-
Molekylmodell av s-trans-formen.
-
Molekylmodell av s-cis-formen.
Användning[redigera | redigera wikitext]
Butadien är en viktig industrikemikalie som används vid tillverkning av syntetgummi. Den polymeriseras till polybutadien som i sig är ett mycket mjukt material, men kan stabiliseras genom att till sätta styren eller akrylnitril, så kallad ABS-plast.
Källor[redigera | redigera wikitext]
- ^ Anslyn, Eric V.; Dennis A. Dougherty (2006). Modern Physical Organic Chemistry. Herndon, Virginia: University Science Books. sid. 115. ISBN 978-1-891389-31-3