Elektrolys
| Den här artikeln behöver källhänvisningar för att kunna verifieras. (2021-11) Åtgärda genom att lägga till pålitliga källor (gärna som fotnoter). Uppgifter utan källhänvisning kan ifrågasättas och tas bort utan att det behöver diskuteras på diskussionssidan. |
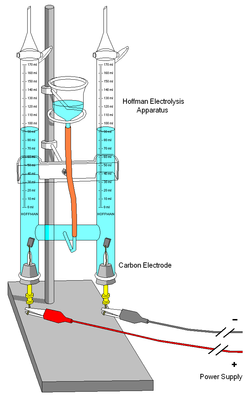
Vid elektrolys används en strömkälla för att driva en redoxreaktion i en, för elektroderna, gemensam elektrolytlösning (lösning som kan leda ström). Elektroner tillförs genom katoden (den negativa polen). Hit vandrar positiva joner som reduceras genom att de mottar elektroner från katodens yta. Vid anoden (den positiva polen) sker på motsvarande sätt en oxidation då de negativa jonerna avlämnar elektroner där.
Vid vattenlösta elektrolyter (aq) reagerar även vattnet. Det är ej endast de fåtaliga OH-- och H3O+-jonerna i vattnet som reagerar. Vattnet reagerar enligt
och
- 2 H2O + 2 e- → H2 + 2 OH- (en reduktion).
Michael Faraday hade uppställt lagarna för elektrolys och infört begreppet joner, utan att veta vad joner egentligen var för något. Det han visste var att de transporterar elektricitet. Det var svensken Svante Arrhenius som löste problemet: Faradays joner var atomer eller atomgrupper med positiv eller negativ laddning. Arrhenius teori innebär att salter sönderdelades i enklare beståndsdelar, joner, när de löses i vatten.
- NaCl(s) → Na+(aq) + Cl-(aq)
Denna elektrolytiska dissociationsteori mötte till en början motstånd. Emellertid bevisade William Bragg med hjälp av röntgenstrålning (röntgendiffraktion) att salter var regelbundet uppbyggda och bestod av joner vilket bekräftade Arrhenius teori.
Användning[redigera | redigera wikitext]
Elektrolys används bland annat till att spjälka vatten i vätgas och syrgas och till att sönderdela natriumklorid i metalliskt natrium och klorgas. Ur aluminiumoxid och kol får man på samma sätt fri aluminiummetall och koldioxid. Galvanisk ytbehandling sker genom elektrolys exempelvis eloxering av aluminium samt elektrolytisk utfällning av exempelvis zink, tenn, kadmium, guld, silver, koppar krom, nickel.
Industriell användning av elektrolys kan vara till exempel förkromning, då krom fälls ut, och rostskyddsbehandling, då kadmium är effektivt att fälla ut. Se udylitisering.
Se även[redigera | redigera wikitext]
 Wikimedia Commons har media som rör Elektrolys.
Wikimedia Commons har media som rör Elektrolys.- Elektroplätering
- Galvanisering
Externa länkar[redigera | redigera wikitext]
 Wikimedia Commons har media som rör Elektrolys.
Wikimedia Commons har media som rör Elektrolys.
