Nitrat
| Den här artikeln behöver fler eller bättre källhänvisningar för att kunna verifieras. (2022-07) Åtgärda genom att lägga till pålitliga källor (gärna som fotnoter). Uppgifter utan källhänvisning kan ifrågasättas och tas bort utan att det behöver diskuteras på diskussionssidan. |
| nitrat | |
 | |
| Systematiskt namn | nitrat |
|---|---|
| Kemisk formel | NO3- |
| Molmassa | 62.00 g/mol |
| SI-enheter & STP används om ej annat angivits | |
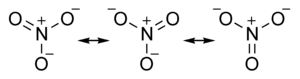
Nitrater är, inom den oorganiska kemin, salter av nitratjonen. Nitratjonen är en sammansatt jon med den kemiska beteckningen NO3-.
Nitratjoner bildas när nitrifikationsbakterier omvandlar ammoniumjoner NH4+ till nitritjoner och sedan vidare till nitratjoner. Nitratjonerna kan sedan omvandlas till kvävgas genom denitrifikation av fakultativt anaeroba bakterier.
Alla metallnitrat är lösliga i vatten. Vissa nitrater är flyktiga, till exempel kopparnitrat (Cu(NO3)2) och kvicksilvernitrat (Hg(NO3)2). Vid upphettning sönderfaller metallnitrat vanligen till metalloxid och kvävedioxid, undantaget natrium- och kaliumnitrat som bildar motsvarande metallnitrit och syre. Ammoniumnitrat sönderdelas vid upphettning till lustgas och vattenånga. Ett viktigt exempel på ett organiskt nitrat är nitroglycerin, som används både inom medicinen och sprängmedelsindustrin.
Finns i[redigera | redigera wikitext]
Gödning[redigera | redigera wikitext]
Nitrat är en viktig beståndsdel i såväl naturgödsel som mineralgödsel. Eftersom nitrat är mycket lättlösligt i vatten kan det lakas ut i vattendrag och hav och där ge problem med övergödning.[1]
Livsmedel[redigera | redigera wikitext]
Nitrat finns naturligt i exempelvis spenat, rödbeta, sallat och ruccola. En del omvandlas i kroppen till nitrit.
Nitrat och nitrit kan finnas i vatten från egen brunn. Troligen på grund av att gödselvatten runnit in i brunnen.
Nitrat och nitrit förekommer även som tillsats i exempelvis charkprodukter för att förhindra uppkomst av livsfarligt botulinumtoxin.[2]
Råd[redigera | redigera wikitext]
Ge inte födoämnen rika på nitrat till spädbarn under ett år. Låt inte smoothies, grönsaksjuice eller andra maträtter innehållande nitratrika födoämnen stå länge framme i rumstemperatur, eftersom det är då nitraterna omvandlas till de betydligt farligare nitriterna.
Läkemedel[redigera | redigera wikitext]
Nitrater finns exempelvis i vissa mediciner mot kärlkramp (angina pectoris). De fungerar kärlvidgande, vilket sänker blodtrycket och på så vis avlastar hjärtat.[3]
Referenser[redigera | redigera wikitext]
- ^ ”sprida gödsel”. jordbruksverket. https://jordbruksverket.se/vaxter/odling/vaxtnaring/sprida-godsel. Läst 31 juli 2022.
- ^ ”Nitrat, nitrit och nitrosaminer”. www.livsmedelsverket.se. https://www.livsmedelsverket.se/livsmedel-och-innehall/oonskade-amnen/nitrat-nitrit-och-nitrosaminer. Läst 31 juli 2022.
- ^ ”Läkemedel vid kärlkramp”. 1177. https://www.1177.se/behandling--hjalpmedel/behandling-med-lakemedel/lakemedel-utifran-diagnos/lakemedel-vid-karlkramp/. Läst 31 juli 2022.
