Propranolol
| Den här artikeln har källhänvisningar, men eftersom det saknas fotnoter är det svårt att avgöra vilken uppgift som är hämtad var. (2019-09) Hjälp gärna till med att redigera artikeln, eller diskutera saken på diskussionssidan. |
| Propranolol | |
 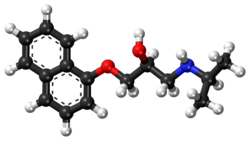 | |
| Systematiskt namn | 1-naftalen-1-yloxy-3-(propan-2-ylamino)propan-2-o |
|---|---|
| Kemisk formel | C16H21NO2 |
| Molmassa | 259.34 g/mol |
| CAS-nummer | 525-66-6 |
| SMILES | CC(NCC(O)COC1=C(C=CC=C2)C2=CC=C1)C |
| Egenskaper | |
| Löslighet (vatten) | 0.0617 (25 °C) g/l |
| Smältpunkt | 96 °C |
| Faror | |
| LD50 | 565 mg/kg |
| SI-enheter & STP används om ej annat angivits | |
Propranolol är en antihypertensiv medicin som agerar på kroppens noradrenerga system. Den minskar aktiviteten hos kroppens sympatiska nervsystem genom att blockera adrenerga beta-receptorer, vilket bland annat leder till sänkt blodtryck.
Propranolol skrivs framförallt ut för att behandla sjukdomar i kardiovaskulära systemet, till exempel hjärtinfarkt, högt blodtryck, angina pectoris, men även för giftstruma, migrän, tumörer i binjuremärgen och tremor. Den har även använts experimentellt mot posttraumatiskt stressyndrom, där den verkar minska symptomen på tillståndet.
Eftersom betablockerare sänker blodsockret, kan propranolol ge hypoglykemi. Det kan också förvärra obstruktiva lungsjukdomar och sänka pH-värdet i blodet. Ökad drömaktivitet och mardrömmar förekommer vid behandling med propranolol. Dess påverkan på blodkärlen kan leda till vita fingrar. Agranulocytos är en allvarlig biverkning som kan uppkomma.
Medicinsk användning
[redigera | redigera wikitext]

Propranolol används för att behandla olika medicinska tillstånd, såsom:
Kardiovaskulär
[redigera | redigera wikitext]- Hypertoni
- Kärlkramp
- Hjärtinfarkt
- Takykardi
- Portahypertension
- Förebygga blödningar och ascites hos Esofagusvaricer
- Ångest
Tidigare var propanolol en av de bästa behandlingar för hypertoni. Eftersom de inte kunde ge lika bra effekt som andra mediciner, särskilt bland de äldre, blev beta-blockeraren nedgraderad till fjärde-klass i juni 2006 i Storbritannien. Fler och fler bevis hos de mest frekvent använda beta-blockerare vid normal dosering har även påvisat att öka risken för Typ 2-diabetes.[1]
Psykiatri
[redigera | redigera wikitext]Propranolol används ibland till för att behandla scenskräck. Dock finns inte lika bra bevis på att behandla andra ångeststörningar.[2] De utförda experiment i andra psykiatriska områden: [3]
- Posttraumatiskt stressyndrom (PTSD) och specifika Fobier
- Förbättringar av sociala förmågor hos personer med Autismspektrumstörning[4]
- Aggressivt beteende av patienter med Hjärnskada[5]
- Behandling för överdrivet drickande av vätskor som orsakas av Polydipsi[6][7]
Syntes
[redigera | redigera wikitext]
Propranolol framställs ur 1-naftol och epiklorhydrin. I första steget öppnas epoxid-ringen upp av nukleofil-attack från OH-gruppen i 1-naftol, samtidigt sker 2 stegs protonöverföring. Vätet som sitter på -OH hamnar nu på epoxidsyret. I det andra steget sker en SN2-reaktion, i det här fallet, en nukleofil substitution av isopropylamin på det kolet som binder till den hyfsat bra lämnande grupp -Cl. Därav bildas den önskade slutprodukten - propranolol.
Man kan även använda sig av en stark bas som NaOH i det undre steget. Den starka basen NaOH hjälper till att deprotonera vätet som är bunden till OH-gruppen i 1-naftol, samtidigt hjälper den till att stabilisera den bildande alkoxid. Den nya natrium-1-naftolat intermediat som har bildats är en bra nukleofil. På samma sätt kommer den att attackera kolet som binder till -Cl på epiklorhydrin och en ny mellanprodukt bildas. Därefter görs en nukleofil-attack av isopropylamin på det elektrofila kolet som sitter på epoxidsyret. Vilket resulterar i en ringöppning och syret protoneras till en alkohol, därav fås slutprodukten - propranolol.
Propranolol är en racematisk blandning – det vill säga, två enantiomerer, R(+) och S(-). S(-)-enantiomeren är ungefär 100 gånger bättre än R(+)-enantiomeren på att blockera adrenerga beta-receptorer.
Syntesen ovan (1) visar ett generellt och billigt sätt att syntetisera propranolol. Men för att undvika racemat har forskare behövt hitta andra sätt. Som till exempel syntesen nedan (2) som är steoreoselektiv, vilket betyder att det mesta av produkten blir S(-)-propranolol. [8]
(I) K2CO3, CH2=CHCH2Br, acetone, reflux, 12 h; 97-99%; (II) cat-OsO4, (DHQD)2-PHAL, K3Fe(CN)6, K2CO3, t -BuOH:H2O, 0 °C, 12 h, 94-98%; 73-90% ee; (III) SOCl2, Et3N, CH2Cl2, 0 °C, 40 min.; 96-99%; (IV) cat. RuCl3.3H2O, NaIO4, CH3CN:H2O, 0 °C, 30 min., 94-98%; (V) LiBr, THF 25 °C, 2-3 h; (VI) 20% H2SO4, Et2O, 25 °C, 10 h; (VII) K2CO3, MeOH, 0 °C, 2 h, 80-85%; (VIII) iPr-NH2, H2O (cat.), reflux, 2 h, 99%.
Referenser
[redigera | redigera wikitext]- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Propranolol, 22 oktober 2011.
Noter
[redigera | redigera wikitext]- ^ Sheetal Ladva (28 juni 2006). ”NICE and BHS launch updated hypertension guideline”. National Institute for Health and Clinical Excellence. Arkiverad från originalet den 24 september 2006. https://web.archive.org/web/20060924003311/http://www.nice.org.uk/download.aspx?o=335988. Läst 11 oktober 2009.
- ^ Steenen, SA; van Wijk, AJ; van der Heijden, GJ; van Westrhenen, R; de Lange, J; de Jongh, A (February 2016). ”Propranolol for the treatment of anxiety disorders: Systematic review and meta-analysis.”. Journal of psychopharmacology (Oxford, England) 30 (2): sid. 128–39. doi:. PMID 26487439.
- ^ ”[40 years beta-adrenoceptor blockers in psychiatry]” (på german). Fortschritte der Neurologie · Psychiatrie 75 (4): sid. 199–210. April 2007. doi:. PMID 17200914.
- ^ ”Blood pressure medicine may improve conversational skills of individuals with autism”. University of Missouri via PsyPost.com. 1 februari 2016.
- ^ ”[Anti-aggressive effect of beta-blockers]” (på french). L'Encéphale 19 (3): sid. 263–7. 1993. PMID 7903928.
- ^ ”The consulting psychiatrist and the polydipsia-hyponatremia syndrome in schizophrenia”. International Journal of Psychiatry in Medicine 24 (4): sid. 275–303. 1994. doi:. PMID 7737786.
- ^ ”Is propranolol effective in primary polydipsia?”. International Journal of Psychiatry in Medicine 28 (3): sid. 315–25. 1998. doi:. PMID 9844835.
- ^ Vinaj Vijayraj Thakur (1 juli 2002). ”ASYMMETRIC SYNTHESIS OF BIOACTIVE MOLECULES AND FORMATION OF C-C, C-N, C-Br, S-O BONDS BY TRANSITION METAL CATALYSIS”. Process Development Division National Chemical Laboratory. Arkiverad från originalet den 9 mars 2017. https://web.archive.org/web/20170309064741/http://ncl.csircentral.net/162/1/th1291.pdf#. Läst 19 februari 2017.



