Extrakorporeal membranoxygenering
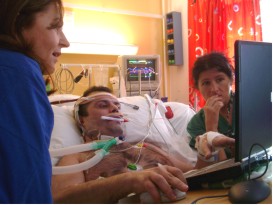
ECMO står för extracorporeal membrane oxygenation, på svenska extrakorporeal membranoxygenering, det vill säga syresättning utanför kroppen genom ett membran. ECMO är en modifierad hjärt- och lungmaskin som ger ett fullständigt utbyte av syre och koldioxid[1], som en konstgjord lunga. Metoden används bland annat vid fall av kongenitalt diafragmabråck eller andra sjukdomar som medför nedsatt lungfunktion [2][3], till exempel komplikationer vid influensa eller covid-19.[4][5]
Typer[redigera | redigera wikitext]
Det finns olika typer av ECMO. De vanligaste är veno-arteriell (V-A) och veno-venös (V-V). I båda metoderna hämtas blod från det venösa flödet och syresätts utanför kroppen. Vid V-A-ECMO återförs blodet till det arteriella systemet och vid V-V-ECMO till det venösa systemet.
Användningsområden[redigera | redigera wikitext]
ECMO används främst i intensivvård för nyfödda som har andningssvårigheter. Behandlingen är framgångsrik i cirka 75 % av fallen. Eftersom nyfödda inte kan behandlas med normal ECMO om de väger mindre än cirka 2 kg kan den inte användas för många prematurt födda. Om för tidigt födda behöver ECMO flygs ett specialutbildat team in som är specialiserat på ECMO för prematurt födda barn. Nyfödda sätts ibland på ECMO på grund av att de saknar ett helt fungerande andningssystem eller på grund av någon annan missbildning men chansen till överlevnad är då endast ungefär 33 %.
Metoden används även i intensivvård för vuxna. ECMO-behandlingen genomförs av ett team av ECMO-specialister som innehåller intensivvårdsläkare, perfusionister, och sjuksköterskor med särskild utbildning.
Tillägg av VV-ECMO har i en systematisk litteraturöversikt[6] som har granskats och kommenterats av SBU visats ge bättre överlevnad än enbart respirator hos vuxna med akut svår lungsvikt, adult respiratory distress syndrome (ARDS).[7] I sällsynta fall kan ECMO övervägas som temporär behandling vid refraktärt hjärtstopp.[8]
Funktion[redigera | redigera wikitext]
En ECMO-maskin liknar en hjärtlungmaskin som är anpassad för användning under längre tid.[7] En hjärt–lungmaskin består i princip av en pump och en konstgjord lunga (så kallad oxygenator) och kan ersätta hjärtats och lungornas funktion under en begränsad tid.[7] Hjärt-lungmaskinen användes för första gången i kliniskt bruk 1953 vid en hjärtoperation. Metoden är utvecklad i USA och den första lyckade ECMO-behandlingen av en vuxen patient utfördes 1971 och av ett spädbarn 1975. ECMO har varit tillgängligt i Sverige sedan slutet av 1980-talet. De ursprungliga oxygenatorerna skadade blodet och kunde endast användas under några timmar.[7]
ECMO fungerar så att en grov kanyl sätts in i personens blodkärl för att suga ut syrefattigt blod. Blodet syresätts i ECMO-apparaten genom att det passerar ett membran som tillför syre och tar bort koldioxid. Sedan förs det syresatta blodet tillbaka till patienten. Kanylen där blodet sugs ut läggs alltid in i en större ven, medan en återförande kanyl kan läggas in antingen i en ven (venovenöst, V-V) eller i en större artär (venoarteriellt, V-A). V-V-ECMO understödjer endast lungfunktionen, medan V-A-ECMO stödjer hela blodcirkulationen.[7] V-A-ECMO medför större risk för blödningar. Den som behandlas med ECMO får antikoagulantia, vanligen heparin, för att hindra blodet från att koagulera.
Syresättning med hjälp av ECMO-behandling gör det möjligt att sänka trycket i personens respirator, så att lungorna löper mindre risk att skadas.[7] Det blir också möjligt för personen att vara mer vaken, så att man kan röra sig, medverka i vården och kommunicera med omvärlden.
Behandlingstid[redigera | redigera wikitext]
ECMO kan användas från några dagar till flera månader.[7] Mediantiden för en vuxen patient ligger omkring 10 dagar.[7] Tidsgränsen för en nyfödd är vanligen cirka 21 dagar. ECMO behandlar inte grundsjukdomen utan understödjer livsviktiga funktioner hos lungorna och hjärtat under tiden som grundsjukdomen behandlas på annat sätt, till exempel med antibiotika. V-V-ECMO kan förse kroppen med syre under flera veckor, vilket ger sjuka lungor tid att läka och undviker risken för tillkommande skador genom mekanisk ventilation. Det kan därför rädda livet för vissa patienter. På grund av de höga kraven på teknisk utrustning, kostnaderna och risken för komplikationer (såsom blödningar på grund av antikoagulantia) anses dock ECMO oftast som en sista utväg.[7]
Se även[redigera | redigera wikitext]
Referenser[redigera | redigera wikitext]
- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia.
- ^ Tomas Wester. Kongenitalt diafragmabråck Karolinska institutet[död länk]
- ^ ”What is an ECMO Machine?”. http://www.wisegeek.com/what-is-an-ecmo-machine.htm. 090720 wisegeek.com
- ^ ”What is Extracorporeal Membrane Oxygenation?”. http://www.wisegeek.com/what-is-extracorporeal-membrane-oxygenation.htm. 090720 wisegeek.com
- ^ Dagens Nyheter 2009-08-26: Fyra livshotande sjuka i influensan
- ^ ”Coronasmittad patient vårdas i Ecmo”. DN.SE. 18 mars 2020. https://www.dn.se/sthlm/coronasmittad-patient-vardas-i-ecmo/. Läst 26 april 2020.
- ^ Munshi, Laveena; Walkey, Allan; Goligher, Ewan; Pham, Tai; Uleryk, Elizabeth M; Fan, Eddy (2019-02-01). ”Venovenous extracorporeal membrane oxygenation for acute respiratory distress syndrome: a systematic review and meta-analysis” (på engelska). The Lancet Respiratory Medicine 7 (2): sid. 163–172. doi:. ISSN 2213-2600. http://www.sciencedirect.com/science/article/pii/S2213260018304521. Läst 5 februari 2020.
- ^ [a b c d e f g h i] ”Extrakorporeal membranoxygenering (ECMO) vid lungsvikt (ARDS)”. www.sbu.se. Statens beredning för medicinsk och social utvärdering (SBU); Swedish Agency for Health Technology Assessment and Assessment of Social Services. 5 februari 2020. https://www.sbu.se/sv/publikationer/sbu-kommentar/extrakorporeal-membranoxygenering-ecmo-vid-lungsvikt-ards/. Läst 5 februari 2020.
- ^ Kim, Su Jin; Kim, Hyun Jung; Lee, Hee Young; Ahn, Hyeong Sik; Lee, Sung Woo (2016-06). ”Comparing extracorporeal cardiopulmonary resuscitation with conventional cardiopulmonary resuscitation: A meta-analysis”. Resuscitation 103: sid. 106–116. doi:. ISSN 0300-9572. http://dx.doi.org/10.1016/j.resuscitation.2016.01.019. Läst 23 augusti 2019.
