Jonselektiv elektrod
En jonselektiv elektrod är en sensor som omvandlar aktivitet hos en jon i en lösning till en potential som kan kvantifieras. Jonselektiva elektroder skiljer sig fundamentalt ifrån metallelektroder genom att dess funktion inte involverar någon redoxreaktion. Det finns huvudsakligen fyra olika typer av jonselektiva elektroder: elektroder med glasmembran, elektroder med kristallmembran, vätskebaserade elektroder samt "compound"-elektroder.
Funktion[redigera | redigera wikitext]
Nyckelegenskapen hos en ideal jonselektiv elektrod är ett tunt membran kapabelt att binda endast den sorts jon man är intresserad av att detektera. I membranet finns det en ligand som idealt endast binder jonen av intresse. Liganden är dock i realiteten inte fullständigt selektiv och binder också andra oönskade joner. Istället får man se till att liganden har hög affinitet för jonen av intresse och låg affinitet för övriga joner. De joner man inte vill mäta, men som binds till membranet ändå kallas störjoner, vilka vid inbindningen ökar elektrodens utslag. Det är dock relativt enkelt att utföra försök för att beräkna störjonens påverkan och sedan kompensera för denna störpåverkan i sina beräkningar.
Exempel på ligand som kan finnas i membranet är valinomycin, som har hög affinitet för kaliumjoner men låg affinitet för störjoner. För att laddningskompensera och skapa en hydrofob miljö i membranet, måste också membranet alltid innehålla hydrofoba anjoner, exempelvis tetrafenylborat.
Jonselektiva elektroder fungerar genom att membranet från början innehåller, som nyss nämnt, en ligand (L) och hydrofoba anjoner (A−). I lösningen som vi syftar till att mäta finns det (förhoppningsvis) det jonslag man vill bestämma koncentrationen av (C+), men förmodligen även störjoner och anjoner. När elektroden doppas i lösningen kommer mätjoner binda in till liganderna i membranet och bilda komplex. Övriga joner, som inte kan vara i den hydrofoba miljön om de inte binder till liganden, kommer att stanna kvar i vattenlösningen med undantag ifrån några få störjoner som också lyckas binda in till liganden.
I membranet har vi nu ligand-mätjon-komplex (LC+), fria ligander (L), de stationära hydrofoba anjonerna (A−) samt några fria mätjoner (C+). De fria mätjonerna är få, och finns i membranet på grund av jämvikten
- .
Dessa fria mätjoner är fria att röra sig, diffundera, ut i vattenlösningen igen eftersom jonerna "trivs bättre", det är mer energetiskt fördelaktigt, att vara lösta i vatten. Men så fort mätjonerna diffunderar till vattenlösningen kommer det bli ett positivt laddningsöverskott i lösningen. Denna obalans ger upphov till en elektrisk potential som hindrar fler joner ifrån att diffundera ut i vattenfasen. Denna elektriska potential uppkommer precis utanför membranets skikt mot vattenfasen och är lika med
- .
Denna ekvation gäller vid 25 °C för samtliga jonselektiva elektroder. E är potentialen och ges i enheten volt, n är analytjonens laddning och mätjonens aktivitet (ungefär koncentration). Genom att ha en potentiometer som kan mäta potential och en referenselektrod att ha som referens kopplade till systemet kan man bestämma den uppkomna potentialen.
För att med formeln sedan kunna beräkna mätjonens aktivitet, , måste man känna till konstantens storlek. Konstantens storlek beror dock av flera faktorer som varierar mellan både olika elektroder och mättillfällen. För att vid just den aktuella mätningen kunna veta dess storlek mäts också potentialen hos prover med redan kända jonhalter, s.k. referensprov. På så vis kan man sätta upp en kalibreringskurva och direkt få reda på aktiviteten av jonen man ville mäta.
Elektroder med glasmembran[redigera | redigera wikitext]
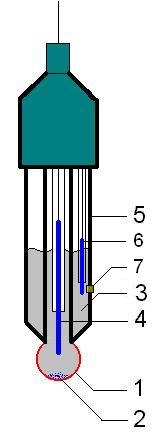
Det vanligaste användningsområdet för jonselektiva elektroder är för pH-mätning. pH är ett mått på koncentrationen vätejoner i en lösning. Sådana mätningar utförs med en elektrod med glasmembran. Allra vanligast att använda vid pH-mätning är en s.k. kombinationselektrod, där både referenselektrod och glasmembranelektroden är inkorporerade i samma kropp.
- glasmembran, elektrodens sensitiva del.
- då innerlösningen ofta är mättad med AgCl kan här ibland bildas en fällning av AgCl.
- innerlösning, vanligtvis 0,1 M HCl mättad med AgCl vid pH-mätning.
- inre referenselektrod, vanligtvis en silver-silver-elektrod eller kalomel-elektrod.
- hölje, tillverkad av icke-ledande glas eller plast.
- referenselektrod, vanligtvis av samma typ som 4.
- porös plugg, som tillåter långsam dränering av elektrolyter ut ur elektroden.
Glasmembranet måste kunna leda en ström. Vanligt glas innehåller kvarts som saknar fria laddningsbärare. För att kunna använda glas dopas det vid tillverkning. Dopning är då man insätter ett kemiskt ämne i strukturen hos ett annat. I detta fall dopas kvarts med metalljoner, såsom litiumjoner, natriumjoner eller kaliumjoner. Dessa metalljoner fungerar sedan som fria laddningsbärare i glaset och sänker därför dess resistans tillräckligt för att användas som glasmembran i elektroden. Dessutom kan glaset nu fungera som en väldigt bra ligand för vätejonerna.
De två referenselektroderna (se 4 och 6 i bilden) ansvarar för att mäta uppkomsten av potential över glasmembranet när vätejonerna som bundit till glasmembranet vill diffundera ut igen. Den uppkomna potentialen beskrivs av ekvationen i avsnittet om den jonselektiva elektrodens funktion och tillåter beräkning av vätejonskoncentrationen i den lösning elektroden doppats i.
Elektroder med kristallmembran[redigera | redigera wikitext]
Generellt består en elektrod med kristallmembran av ett ytterhölje med ett inkorporerat kristallmembran. Kristallmembranet gränsar liksom membranet för en elektrod med glasmembran både mot en innerlösningen och den yttre mätlösningen. Inuti höljet finns förutom den stabiliserande innerlösningen också en referenselektrod, ofta i form av en silver-silver-elektrod. Elektroden är också kopplad till en potentiometer med möjlighet att mäta elektrisk spänning över membranet.
En mycket vanlig jon att mäta koncentrationen av med hjälp av en elektrod med kristallmembran är fluoridjonen (F−). Principen vid mätning av denna jon, som kan anses som generell princip för hur en elektrod med kristallmembran fungerar, bygger på användandet av en lantanfluoridkristall (LaF3). Denna kristall dopas med europiumjoner (Eu2+). Dopingen innebär här addition av små mängder Eu2+-joner till kristallen, vilka ersätter vissa lantanjoner (La3+) i kristallstrukturen. I och med att Eu2+-jonerna har en 2-värd positiv laddning, att jämföra med La3+-jonernas 3-värda, så binder denna en F− färre (två styck, jämfört med tre). Detta skapar en förändring i kristallstrukturen, och vakanta platser skapas där en F−-jon tidigare var bunden.
Innerlösningen i elektroden består av 0,1 M natriumfluorid och 0,1 M natriumklorid för att stabilisera elektroden. Istället för att, som i fallet med elektroder med glasmembran, binda in till membranet kan istället F−-jonerna migrera in i kristallen. Migrationen, vilket här kan översättas till vandrandet, genom kristallen möjliggörs av de vakanser i kristallen dopningen skapat. Fluoridjonen "hoppar" helt enkelt till en vakant plats, och lämnar en ny vakans bakom sig. Enligt principen för jonselektiva elektroder möjliggörs på så vis skapandet av en elektrisk potential över membranet då elektroden doppas i en lösning som ska mätas innehållande fluoridjoner.
Referenser[redigera | redigera wikitext]
- Harris, Daniel C.. Quantitative Chemical Analysis (7:e uppl., 2007). ISBN 9780716776949




