Covid-19-vaccin



Ett covid-19-vaccin är ett vaccin som är avsett att ge immunitet mot sjukdomen covid-19. När covid-19-pandemin bröt ut fanns redan arbete med att ta fram vaccin mot två andra sjukdomar som orsakas av coronavirus, sars och mers. Man hade därför redan ganska god kunskap om coronavirusens struktur och egenskaper, vilket gjorde vägen till fungerande covid-19-vaccin kortare.[1]
Forskning om vaccin och andra läkemedel[redigera | redigera wikitext]
Över hela världen utfördes ett intensivt arbete för att ta fram vaccin och läkemedel mot covid-19. Forskare började samarbeta på nya sätt och en stor del av världens samlade forskarkår inom läkemedel fokuserade på samma sak och nästan all annan forskning avbröts eller pausades.[2] Detta ledde till flera utvecklade vaccin mot pandemin. Den globala läkemedelsindustrin lyckades att på mindre än ett år ta fram vacciner som kunde börja användas i slutet av 2020.
Arbetet i Sverige[redigera | redigera wikitext]
Professorn i biomedicinsk analys Matti Sällberg ledde det svenska arbetet med ett DNA-vaccin mot sars-cov-2 tillsammans med Ali Mirazimi och Gustaf Ahlén.[3] Under tio år hade Sällberg arbetat med att utveckla andra dna-baserade vaccin mot sjukdomar som hepatit B och Krim-Kongo hemorragisk feber som sprids med fästingar. Karolinska institutet projekt ”Open Corona” fick 30 miljoner kronor från EU för att utveckla ett vaccin mot sars-cov-2.[4] Forskningssamarbetet skedde tillsammans med företagen Cobra Biologics som producerar plasmiderna och Adlega som utför toxikologiska studier.[5]
Vaccinkandidater[redigera | redigera wikitext]
I mitten av december 2020 var totalt 57 vaccinkandidater föremål för kliniska studier, varav 40 i fas I – II-studier och 17 i fas II – III-studier. I fas III-studier visade flera covid-19-vacciner hög effektivitet, med en skyddseffekt kring 95 % jämfört med ingen behandling.[6][7] EU (Europeiska läkemedelsmyndigheten, EMA) och USA har godkänt två mRNA-vacciner (Comirnaty från Pfizer/Biontech och COVID-19 Vaccine Moderna från Moderna). Utöver det har fem ytterligare vaccin godkänts av vissa nationella läkemedelsmyndigheter: två konventionella inaktiverade vacciner (BBIBP-CorV från Sinopharm och Coronavac från Sinovac) och tre virusvektorvacciner (Sputnik V från Gamaleya Research Institute, Vaxzevria från Oxfords universitet och Astra Zeneca samt Ad26.COV2.S från Janssen-Cilag International).
Massvaccineringen inleds[redigera | redigera wikitext]
Massvaccinering påbörjades i Storbritannien den 8 december 2020 och i Sverige den 27 december 2020.[8][9] Många länder har genomfört stegvisa distributionsplaner som prioriterar de som har störst risk för allvarliga symptom, som äldre, och de som har hög risk för exponering och överföring, såsom sjukvårdspersonal.[10] Den 7 februari 2021 hade cirka 128 miljoner doser covid-19-vaccin givits över hela världen baserat på officiella rapporter från nationella hälsovårdsmyndigheter.[11] Pfizer, Moderna och Astra Zeneca förutspådde en tillverkningskapacitet på 5,3 miljarder doser 2021, som skulle kunna användas för att vaccinera cirka 3 miljarder människor (eftersom vaccinerna kräver två doser för en skyddande effekt mot covid-19). I december 2020 hade mer än 10 miljarder vaccindoser förbeställts av länder.[12] Ungefär hälften av dessa doser hade beställts av höginkomstländer, vars invånare endast utgör 14 % av världens totala befolkning.[13]
Bakgrund[redigera | redigera wikitext]
Med början av januari 2020, omedelbart efter att viruset sars-cov-2 sekvenserats Kina, sjösattes ett antal utvecklingsprojekt för ta fram vaccin mot covid-19. Världshälsoorganisationen (WHO) uttalade i februari att ett vaccin inte skulle bli tillgängligt på mindre än 18 månader, men det visade sig gå snabbare. Bland andra Coalition for Epidemic Preparedness Innovation finansierade tidigt under 2020 utveckling av utvalda vaccinkandidater. I maj 2020 organiserade WHO en tv-sändning för att samla in 80 miljarder kronor från fyrtio länder för att stödja snabb utveckling av vacciner.
I början av augusti 2020 var 100–150 vaccinkandidater under utveckling, beroende av hur man räknar, varav 23[14] – 31[15] i kliniska försök. De som kommit längst var då Astra Zeneca och Oxfords universitet (Jenner Institute och Oxford Vaccine Group) med vaccinet AZD1222, med påbörjade fas III-försök i juni.[14] Ytterligare ett fåtal företag hade sommaren 2020 vaccinkandidater i, eller med långtgående förberedelser för, fas III-försök – till exempel Pfizer/Biontech och Moderna.
Världshälsoorganisationen listade den 8 december 2020 52 vaccinkandidater, vilka då genomgick kliniska studier i någon fas, varav 13 i slutfasen, fas III. Dessutom fanns 162 vaccinkandidater i preklinisk utvärdering.[16]
Internationellt samarbete[redigera | redigera wikitext]
Det globala samarbetet för att påskynda utveckling, produktion och rättvis tillgång till det nya covid-19-vaccinet (COVID-19 Tools Accelerator (ACT Accelerator är ett G20-initiativ som tillkännagavs den 24 april 2020. [17]
Den 10 september 2021 samlades FN och Europeiska unionen och då inledde ACT-Acceleratorns arbete, vilket hade fått 2,7 miljarder dollar av de totalt 35 miljarder dollar som ansågs behövas för att säkra de 2 miljarder covid-19-vaccindoser, 245 miljoner behandlingar och 500 miljoner tester som bedömdes nödvändiga för att förkorta pandemin och påskynda den ekonomiska återhämtningen.[18] Under Trump-administrationen drog USA tillbaka sitt stöd till WHO och valde att inte stödja ACT Accelerator.[19] ACT Accelerator ska ses som ett stöd till vetenskapen och öka samarbetet om kunskap samt resurser.[20]:
I december 2020 hade 2,4 miljarder dollar samlats in för ACT Accelerator. Det innebar att nio vaccinkandidater var finansierade av COVAX och CEPI. Detta är världens största vaccinportfölj för Covid-19 med totalt 189 länder som anslutit sig till den slutliga utplaceringsplanen.[21][22]
Tidigare 2020 hade WHO samlat in 8,8 miljarder dollar från ett fyrtiotal länder för påskynda vaccvinutveckling.[23] I december donerade Bill Gates stiftelse ytterligare 2250 miljoner dollar med målet att "stödja leverans av nya Covid-19 test, behandlingar och vacciner, särskilt i låg- och medelinkomstländer". [24][25]
Global Research Collaboration för Infectious Disease Prepared samarbetar med WHO och medlemsländerna för att prioritera finansiering av specifik forskning för covid-19-vaccin och samordnas mellan de internationella finansierings- och forskningsorganisationerna för att uppdatera information om vaccinframsteg och undvika dubbel finansiering.[26]
Vaccinmekanism[redigera | redigera wikitext]
För mer eller mindre varje vaccintyp finns det någon forskargrupp som försöker utveckla ett vaccin av den typen mot covid-19. De som först fick godkännande ingår i den så kallade tredje generationens vacciner som istället för proteiner innehåller genetiskt material, och låter kroppens egna celler tillverka proteinerna.
De två tekniker som först lyckades använde antingen mRNA som förs in i cellerna i fettpartiklar, liposomer, eller adenovirus som virusvektor för att föra in DNA i cellen som kodar för ett av det sjukdomsframkallande virusets proteiner. Oftast har man använt sars-cov-2:s "spike"-protein (tagg-protein), som det behöver för att ta sig in i celler.[27]
Två tredje-delar av biverkningar av covid-vaccin bedöms vara noceboeffekt.[28][29]
mRNA-baserade vaccin[redigera | redigera wikitext]
Dessa vaccin, bestående av mRNA i lipidhölje, har visat sig ha god effekt, men har nackdelen att de måste förvaras och transporteras i fryst skick i mycket låga temperaturer.
Immunitetens varaktighet[redigera | redigera wikitext]
Oavsett om immunitet mot sars-cov-2 uppkommit genom infektion eller vaccin är det osäkert hur länge den varar. Studier av immuniteten mot de sedan tidigare cirkulerande coronavirusen (HCoV-229E, HCoV-OC43, HCoV-NL63, HCov-HKU1) talar för att den kanske inte varar mer än högst ett år[30][31]. Genom ansamling av mutationer i virusets arvsmassa kan dess proteiner komma att förändras så mycket att vaccinens skyddseffekt avtar.[32][33][34][35] Flera vaccintillverkare bedriver forsknings- och utvecklingsarbete för att kunna förändra sin vacciner med hänsyn till detta[36][37]. Den europeiska läkemedelsmyndigheten EMA kommer därför att skapa ett regelverk för hur sådana modifierade vacciner ska kunna godkännas i en förkortad process.[38]
Kandidater till vaccin mot covid-19[redigera | redigera wikitext]

Redan i mitten av maj 2020 befann sig omkring över ett hundra vaccinkandidater under utveckling som antingen bekräftade aktiva projekt eller i preklinisk utvecklingsfas.[39][40] Enligt New York Times var den 20 juli 18 vaccinkandidater i fas 1, tolv i fas 2 och fyra i fas 3.[41] I december 2020 fanns närmare 290 vaccinkandidater i något skede av utveckling.[42]
I december 2020 hade ansökningar om akutlicenser inlämnats av Pfizer/Biontech och Moderna till bland andra Europeiska läkemedelsmyndigheten. Pfizer/Biontech har erhållit akutlicens i Storbritannien och ett vaccinationsprogram inleddes där den 8 december.[43] Någon form av tillstånd har därefter lämnats av bland andra USA, Europeiska unionen, Kanada, Schweiz och Bahrain.
Under fas I testas främst för säkerhet och preliminär dosering på några dussin friska försökspersoner, medan det under fas II utvärderas immunogenicitet, dosnivåer (effekt baserat på biomarkörer) och negativa effekter av kandidatvaccinet, vanligtvis på hundratals människor. I fas II utförs preliminär säkerhets- och immunogenicitetsundersökning. Denna är randomiserad, placebokontrollerad och utförs på flera platser, samtidigt som man fastställer mer exakt dosering. Fas III-studier är längre och involverar fler deltagare, inklusive en kontrollgrupp, samtidigt som negativa effekter efterforskas.
Framtagningsprocessen[redigera | redigera wikitext]
Vaccinkandidater har tagits fram och godkänts och tillverkats mycket snabbt historiskt sett. Världshälsoorganisationen förutspådde i februari 2020 att ett vaccin inte skulle bli tillgängligt på mindre än 18 månader, men det visade sig gå snabbare. Redan i december 2020 hade vacciner godkänts av de tongivande aktörerna i västvärlden: Food and Drug Administration och Europeiska läkemedelsmyndigheten. Det har pekats på åtminstone ett tiotal tekniska anledningar till snabbheten i dessa förfaranden[44]:
- Fackorganisationer, som den 2017 bildade Coalition for Epidemic Preparedness Innovation (CEPI), var redan beredda på att en pandemi skulle inträffa förr eller senare. Likaså hade företag och institutioner som Biontech, Moderna och Jenner Institute vid Oxfords universitet sedan flera år utvecklat nya tekniker för att skapa vacciner, baserade på det infektuösa ämnets genetiska kod.
- På Fudanuniversitetet i Shanghai identifierades det nya SARS-CoV-2-viruset på ett tidigt stadium och gjordes sekvensering av virusets RNA samt publicerade resultatet av detta. För de vaccintyper som baseras på RNA och på virala vektorer räcker det med information om den genetiska koden för att påbörja vaccinforskning.
- Forskningsinstitutionerna fick omedelbar och omfattande finansiering.
- De administrativa processerna i samband med kliniska försök skedde snabbare än vanligt.
- Kliniska försök organiserade snabbare än vanligt.
- Forskningsdata från kliniska försök insamlades och hanterades, till skillnad från tidigare, elektroniskt och spreds snabbt.
- Rekryteringen till de kliniska försöken gick snabbt på grund av stort antal volontärer.
- Den stora spridningen av covid-19 i den andra vågen gjorde att det blev snabba resultat av de kliniska försöken i fas III.
- De tidiga vaccinkandidaterna hade ett högt skyddsvärde, det vill säga var effektiva. Detta tillät slutsatser av fas III-försöken vid en tidigare tidpunkt, än vad som annars skulle varit fallet.
- De tillståndsgivande myndigheterna följde pågående försök i realtid, vilket innebar att de mycket snabbare kunde göra slutlig prövning än vid ett normalt förfarande.
- Tillverkning av vaccin påbörjades långt innan godkännande av vaccinkandidater.
Egenskaper för utvalda vacciner[redigera | redigera wikitext]
Källa: BBC[45]
| Läkemedelsföretag | Vaccin/vaccinkandidat | Teknik | Antal doser | Förvarings- och distributionskrav | Skyddsvärde (preliminära resultat från fas III-försök) |
Ungefärligt pris per dos |
|---|---|---|---|---|---|---|
| Moderna | Spikevax | Budbärar-RNA | 2 | - 15 till - 25 grader C (djupfrys eller kryofrys, lägst - 40 grader C).[46] | 95%[6] | cirka 33 US dollar |
| Astra Zeneca i samarbete med Oxfords universitet | Vaxzevria I Indien Covishield (tidigare AZD 1222 och ChAdOx1 nCoV-19) |
Adenovirus som vektor |
2 | Kylskåpstemperatur, 2 till 8 grader C.[47] | 70%[48] | cirka 4 US dollar |
| Pfizer och Biontech | Comirnaty (Pfizer BioNTech Covid-19 Vaccine) Tidigare BNT162b2 Biontech, i samarbete med Pfizer |
Budbärar-RNA | 2 | Högst - 60 grader C (kryofrys eller torris).[49]
Högst - 15 grader C (djupfrys eller kryofrys) i högst 2 veckor.[50] |
95%[7] | cirka 20 US dollar
|
| Janssen-Cilag International | Ad26.COV2.S Janssen-Cilag International |
Adenovirus som vektor |
2 | Kylskåpstemperatur | 67% [51] | |
| Gamaleja-institutet för epidemiologi och mikrobiologi | Sputnik V | Adenovirus som vektor |
2 | Kylskåpstemperatur (i torr form) | 92%[52] | cirka 10 US dollar |
| Sinopharm | BBIBP-CorV | Inaktiverat virus | 2 | Kylskåpstemperatur | 79% | |
| Sinovac Biotech | Coronavac | Inaktiverat virus | 2 | Kylskåpstemperatur | 50,4 % (resultat från Brasilien)[53] | |
| Bharat Biotech | Covaxin | Inaktiverat virus | 2 | Kylskåpstemperatur | Ej publicerat per 22 januari 2021[54] |
Godkännande[redigera | redigera wikitext]

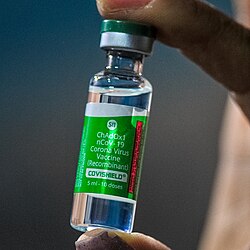
Aktuell status för samtliga vaccinkandidaters vetenskapliga studier inför godkännande framgår av WHO:s dokument "Draft landscape and tracker of COVID-19 candidate vaccines".[55]
Gamaleja-institutets Sputnik V[redigera | redigera wikitext]
- Gam-Covid-Vax (ryska: Гам-КОВИД-Вак), eller Sputnik V (ryska: Спутник V), är ett ryskt vaccin mot covid-19, som utvecklats av Gamaleja-institutet för epidemiologi och mikrobiologi i Moskva i Ryssland.[2] Utvecklingen finansieras av den ryska statliga investeringsfonden RDIF. Per 2021-01-28 är Sputnik V godkänt för emergency use (EUA) i: Ryssland, Algeriet, Argentina, Bolivia, Förenade Arabemiraten, Guinea, Iran, Pakistan, Palestina, Paraguay, Serbien, Turkmenistan, Ungern, Venezuela och Vitryssland. Den 4 mars 2021 påbörjades löpande granskning av EMA för ett eventuellt godkännande för användning inom EU,[56] men frågan om ett godkännande uppgavs i juni 2021 inte kunna tas upp för prövning förrän tidigast i september.
- Ungern och Slovakien har använt Sputnik V i sina vaccinationsprogram, trots att detta inte godkänts av Europeiska läkemedelsmyndigheten.
Comirnaty (Pfizer BioNTech COVID-19 Vaccine)[redigera | redigera wikitext]
- Pfizer och Biontechs covid-19-vaccin, Comirnaty, tidigare BNT162b2, fick i december akuttillstånd ("Emergency Use Authorization") för försäljning av ”Medicines and Healthcare products Regulatory Agency" i Storbritannien[57] samt av Bahrain[58], Saudiarabien och Mexiko. Det säljs även under varunamnet Tozinameran.
- Den 9 december 2020 lämnade Kanadas tillståndsmyndighet Health Canada att normalt tillstånd för vaccinet i Kanada.[59][60] Massvaccinering påbörjades i Storbritannien den 8 december 2020.[8] Food and Drug Administration gav den 11 december Biontechs och Pfizers vaccinkandidat BNT162b2 akuttillstånd för försäljning.[61] Vaccinet godkändes för av EU-kommissionen för akutanvändning i EU:s medlemsländer, med vissa förbehåll, den 21 december 2020, efter ett positivt beslut av Europeiska läkemedelsmyndighetens kommitté för humanläkemedel samma dag.[62].
Moderna Spikevax[redigera | redigera wikitext]
- Tillstånd för akutförsäljning av Spikevax, tidigare mRNA-1273, i USA lämnades av Food and Drug Administration den 18 december 2020.[63] Den 6 januari 2021 godkändes vaccinet för användning i EU på EMA:s rekommendation.[64]
Astra Zenecas Vaxzevria[redigera | redigera wikitext]
- Vaccinet godkändes för användning i Storbritannien den 30 december 2020.[65] Indiska myndigheter gav godkännande för vaccinet, som i Indien går under varumärket Covishield och tillverkas av Serum Institute of India, den 3 januari 2021.[66][54] EU godkände användningen av vaccinet den 29 januari 2021 efter rekommendation av EMA.[67]
Ad26.COV2.S Janssen-Cilag International[redigera | redigera wikitext]
- Tillstånd för akutförsäljning av Ad26.COV2.S, i USA lämnades av Food and Drug Administration den 27 februari 2021.[68] EU godkände användningen av vaccinet den 11 mars 2021 efter rekommendation av EMA.[69]
Sinopharms BBIBP-CorV[redigera | redigera wikitext]
- Förenade Arabemiraten godkände Sinopharms BBIBP-CorV för akutanvändning i september 2020 och för allmän användning i december. Kinas hälsovårdsmyndigheter godkände vaccinet 31 december 2020 för allmänt bruk.[70] Tillstånd för akutanvändning har också lämnats i Bahrain i november[71]
Bharat Biotechs Covaxin[redigera | redigera wikitext]
- Godkännande för akutanvändning lämnades av indiska myndigheter den 3 januari 2021.[66]
[redigera | redigera wikitext]
- Godkännande för akutanvändning lämnades av indonesiska myndigheter den 10 januari 2021.[72] Turkiet, Brasilien, Chile, Colombia, Uruguay och har därefter också godkänt vaccinet för akutanvändning. Kina godkände vaccinet för allmänt bruk den 6 februari 2021.[73]
Förhandsavtal om leveranser mellan EU och läkemedelsföretag[redigera | redigera wikitext]
EU har för medlemsstaternas räkning under andra halvåret 2020 (till och med 10 december) slutit förhandsavtal om leveranser med Pfizer, Moderna, Astra Zeneca, Janssen-Cilag och Curevac. Ett optionsavtal har också träffats med Sanofi, men utvecklingen av Sanofis Pasteurs och Glaxo Smith Klines vaccinkandidat har försenats till åtminstone hösten 2021, efter otillfredsställande resultat av fas I–II-studien.[74]
Vaccinkandidater i process för godkännande av Europeiska unionen[redigera | redigera wikitext]
| Vaccinkandidat och läkemedelsföretag |
Löpande granskning igångsatt |
Process för villkorat försäljnings-tillstånd påbörjad |
Granskning av Europeiska läkemedelsmyndighetens vetenskapliga kommitté för humanmedicin genomförd |
Godkännande av EU-kommissionen fattat |
Anmärkningar |
|---|---|---|---|---|---|
| Spikevax Moderna |
16 november 2020[75] | 1 december 2020[76] | 6 januari 2021[77] | 6 januari 2021[64] | Lagring och distribution: - 15 till - 25 grader C, lägst - 40 grader C
|
| Vaxzevria (tidigare AZD 1222 och ChAdOx1 nCoV-19) Astra Zeneca i samarbete med Oxfords universitet |
1 oktober 2020[78] | 12 januari 2021[79] | 29 januari 2021[80] | 29 januari 2021[67] | Lagring och distribution: kylskåpstemperatur, 2 till 8 grader C
|
| Comirnaty (Pfizer BioNTech COVID-19 Vaccine) Tidigare BNT162b2 Biontech, i samarbete med Pfizer |
6 oktober 2020[82] | 1 december 2020[83] | 21 december 2020[84] | 21 december 2020[62] | Lagring och distribution: högst -60 grader C, högst - 15 grader C i högst 2 veckor.[50]
|
| Ad26.COV2.S Janssen-Cilag International (Johnson & Johnson) |
1 december 2020[86] | 16 februari 2021[87] | 11 mars 2021[51] | 11 mars 2021[69] | Vaccin med en injektion. Lagring och distribution: - 15 till - 25 grader C. Kylskåpstemperatur, 2 till 8 grader C i högst 3 månader |
| Nuvaxovid (tidigare NVX-CoV2373) Novavax/Amerikanska regeringen |
2 februari 2021[89] | 17 november 2021[90] | 20 december 2021[91] | 20 december 2021[92] | Lagring och distribution: kylskåpstemperatur |
| Sputnik V Gamaleja-institutet för epidemiologi och mikrobiologi, Rysslands nationella förmögenhetsfond |
4 mars 2021[93] | Lagring och distribution: kylskåpstemperatur. | |||
| Coronavac Sinovac Biotech |
5 april 2021[94] | Lagring och distribution: kylskåpstemperatur | |||
| Vidprevtyn Sanofi Pasteur/Glaxo Smith Kline |
20 juli 2021[95] | Lagring och distribution: kylskåpstemperatur | |||
| VLA2001 Valneva SE/Dynavax Technologies Corporation |
2 december 2021[96] | Lagring och distribution: kylskåpstemperatur |
Vacciner som godkänts av Food and Drug Administration i USA[redigera | redigera wikitext]
| Vaccin och läkemedelsföretag |
Godkännande för akutförsäljning (Emergency use authorization – EUA) |
Begränsning av tillstånd | Generellt godkännande | Anmärkningar |
|---|---|---|---|---|
| Pfizer BioNTech Covid-19 vaccine, i Europa under varumärket Comirnaty Pfizer och Biontech |
11 december 2020[97] | För personer som är minst 16 år gamla | Lagring och distribution: högst -60 grader C
| |
| Spikevax Moderna |
18 december 2020[63] | För personer som är minst 18 år gamla under akutlicens. | Lagring och distribution: - 15 till - 25 grader C, lägst - 40 grader C | |
| Ad26.COV2.S Janssen-Cilag International (Johnson & Johnson) |
27 februari 2021[68] | För personer som är minst 18 år gamla under akutlicens. | Vaccin med en injektion. Lagring och distribution: kylskåpstemperatur |
Tekniker för framställning av vaccin[redigera | redigera wikitext]

1. mRNA som kodar för ett av virusets gener
2. Genetiskt rekombinerat virusprotein, vad gäller sars-cov-2 dess spikeprotein
3. Viruxvektor som för in en av virusets gener i den vaccinerades celler.
Hösten 2020 skedde utvecklingsarbete på nio olika tekniska plattformar.[förtydliga] Flertalet av dessa var inriktade på det pandemiorsakande viruset sars-cov-2:s spikeprotein, som viruset behöver för att kunna ta sig in i människans celler. Plattformar[förtydliga] som använts 2020 inbegriper nukleinsyretekniker (modifierat budbärar-RNA och DNA), icke-replikerande virala vektorer, peptider, hybrid-DNA, levande försvagat virus och inaktiverat virus.
De flesta metoder som använt för att ta fram covid‑19-vaccin skiljer sig från de vaccin som tidigare funnits tillgängliga.
| Tekniker | Antal vaccinkandidater |
Antal kandidater i kliniska försök på människor |
|---|---|---|
| RNA-baserat | ||
| DNA-baserat | ||
| Icke-replikerande viral vektor | ||
| Replikerande viral vektor | ||
| Inaktiverat virus | ||
| Levande, men försvagat virus | ||
| Protein-subenhet | ||
| Virusliknande partikel | ||
| Andra och ej kända tekniker[förtydliga] |
Vaccinkandidater under kliniska studier i fas II eller fas III under 2020[redigera | redigera wikitext]
(Uppdaterat den 14 december 2020[99])
| Fas III: orange, Fas II: gul, Godkännande: grön | ||||||
|---|---|---|---|---|---|---|
| Vaccinkandidat och utvecklare/partner |
Teknik | Försöksfas och antal deltagare |
Land som försök genomförs i |
Period för försök |
Godkänt i något land (akut eller generellt) |
Anmärkningar |
| Ad5-nCoV CanSino Biologics, Institute of Biotechnology of the Academy of Military Medical Sciences |
Rekombinerat adenovirus, typ 5-vektor | Fas III | Kina, Mexiko | Kina | Godkänd för Fas I i Kina i slutet av juni 2020[100]
Fas III-försök inledda i Mexiko i november 2020.[101] | |
| Vaxzevria (tidigare AZD1222 och ChAdOx1 nCoV-19) Oxfords universitet (Jenner Institute och Oxford Vaccine Group), Astra Zeneca |
Adenovirus som vektor | Fas III | Fas III genomförd | Bland annat Storbritannien och Indien | Positiva tidigare Fas 1–2-resultat publicerade den 20 juli 2020 [102] Resultat av fas III publiceras i The Lancet i december 2020 Ansökan om nödlicens i Storbritannien lämnad | |
| Comirnaty, tidigare BNT162b2 Biontech, Pfizer, Fosun Pharma |
mRNA-teknik | Fas III | Tyskland, USA upp till 30.000 |
Fas III genomförd Juli-augusti 2020–[103] |
Bland annat USA och EU | Studie påbörjad i Tyskland i april och i USA i maj
[104] |
| Coronavac Sinovac Biotech, Bio Farma[105] |
Inaktiverat virus | Fas III | Kina Indonesien 160[105] |
April 2020– ?[105] |
Indonesien[106] Turkiet, Brasilien, Chile, Colombia, Uruguay och har därefter också godkänt vaccinet för akutanvändning. Kina godkände vaccinet för allmänt bruk den 6 februari 2021.[107] | |
| INO-4800 Inovio Pharmaceuticals, Coalition for Epidemic Preparedness Innovation, Korea National Institute of Health, International Vaccine Institute |
DNA-plasmid, åstadkommen genom elektroporering | Fas II | USA, Sydkorea | Positiva preliminäre resultat av fas 1 annonserades den 30 juni 2020, tillsammans med planer på fas 3[108] | ||
| Spikevax, tidigare mRNA-1273 Moderna, National Institute of Allergy and Infectious Diseases under National Institute of Health |
mRNA-teknik | Fas III 30.000 |
USA USA |
Fas III avslutad Juli 2020[109] |
USA och EU | Preliminära resultat av fas 1 publicerade den 14 juli 2020.[110] Planer för fas III från juli 2020 annonserade den 1 juni 2020.[109] Resultat av fas 3 ej publicerade (december 2020) |
| namnlös Sinopharm Groups Wuhan Institute of Biological Products |
Inaktiverat virus | Fas III | Kina | Fas II registrerad för över 1 000 deltagare. | ||
| BBIBP-CorV Sinopharm Groups Beijing Institute of Biological Products |
Inaktiverat virus | Fas III | Kina | Bland annat Kina och Förenade arabemiraten | Godkänt för användning av Förenade arabemiraten i december 2020[111] Använd för bland annat utlandsarbetande kineser hösten 2020. Generellt tillstånd begärt i Kina i november 2020.[111] | |
| Ad26.COV2.S Janssen Pharmaceutical Companies (Johnson & Johnson)/Beth Israel Deaconess Medical Center |
Adenovirus som vektor | Fas III | USA | |||
| Covaxin, tidigare BBV 152[112] Bharat Biotech/Indian Council of Medical Research |
Inaktiverad helvirion | Indien | Indien | Indien | Fas III-studie påbörjad i november 2020. Godkänt av indiska myndigheter den 3 januari 2021.[66] | |
| NVX-CoV2373 Novavax/Amerikanska regeringen[113] |
Rekombinerade peplomerer | Fas III | Australien | Maj 2020– | Fas III-försök inledda omkring årsskiftet 2020/2021.[114] | |
| namnlös[115][116] Medicago Inc. i Quebec City i Kanada |
Växtbaserad (nicotiana benthamiana) teknik med rekombinerad "coronaviruslik partikel" | Fas III | Kanada | |||
| CVnCoV[117][118] CureVac AG, Coalition for Epidemic Preparedness Innovation |
mRNA-teknik | Fas III | Tyskland, Belgien | Fas III påbörjad december 2020. Interimsrapport i juni 2021 visat på 47 % skyddseffekt, vilket understiger krav för godkännande. EMA meddelade 2021-10-12 att CureVac drar tillbaka vaccinkandidaten från den europeiska godkännandeprocessen[119] | ||
| namnlös Anhui Zhifei Biopharmaceutical/Institute of Microbiology, Chinese Academy of Sciences |
Rekombinerad protein | Fas III | Kina | |||
| Sputnik V, eller Gam-Covid-Vak[120] Gamaleja-institutet för epidemiologi och mikrobiologi/Rysslands nationella förmögenhetsfond[121] |
Adenovirus som vektor | Fas II | Ryssland 40.000 | Ryssland | Ryssland godkände vaccinet den 11 augusti 2020 för en period fram till 31 december 2020, utan att fas 3-studie ännu genomförts.[122] [123]. Första granskade data publicerade i The Lancet 2021-02-02[124]. | |
| namnlös Beijing Wantai Biological Pharmacy/Xiamen University |
Influensavirusabaserad receptor-bindande mRNA | fas II | Kina | |||
| namnlös West China Hospital/Sichuan University |
Influensavirusbaserad receptor-bindande mRNA | fas II | Kina | |||
| Vidprevtyn Sanofi Pasteur/Glaxo Smith Kline |
Proteinsubenhet, spikeprotein | Fas I+II Fas I+II |
Frankrike | Kombinerad fas I- och fas II-studie. Utvecklingen har försenats till åtminstone hösten 2021, efter otillfredsställande resultat av fas I–II-studien.[74] | ||
| VLA2001 Valneva SE/Dynavax Technologies Corporation |
Inaktiverat virus, odlat i cellinjen Vero | Fas I+II | Storbritannien | December 2020- | Kombinerad fas I- och fas II-studie. | |
| ABNCoV2 Bavarian Nordic/AdaptVac |
Virusliknande partikel | Fas I+II | Nederländerna | Mars 2021- | Kombinerad fas I- och fas II-studie. | |
Andra vaccinkandidater, i fas I-studie eller i preklinisk utvärdering, i urval[redigera | redigera wikitext]
| Fas I:grön | |||||
|---|---|---|---|---|---|
| Vaccinkandidat och utvecklare/partner |
Teknik | Försöksfas och antal deltagare |
Land som försök genomförs i |
Period för försök |
Anmärkningar |
| namnlös[125] Imperial College London |
mRNA-teknik[126] | Fas I 300 |
Storbritannien | Juli 2020– | |
| Covid-19/aAPC Shenzhen Geno-Immune Medical Institute[127] |
Lentivirus som vektor | Fas I 100 |
Kina | Mars 2020– | |
| LV-SMENP-DC Shenzhen Geno-Immune Medical Institute[128] |
Vaccin med dendritceller som modifierats med lentivirus som vektor |
Fas I 100 |
Kina | Mars 2020– | |
| bacTRL-Spike Symvivo Corporation, University of British Columbia, Dalhousie University |
DNA, bakteriellt medium (oralt) | Fas I 84 |
Kanada | April 2020–december 2021 | |
| COVAX-19 Vaxine Pty Ltd., Flinders University i Adelaide i Australien |
Rekombinerat protein | Fas I 40 |
Australien | Juni 2020– | |
| PittCoVacc[129] University of Pittsburgh |
Proteinsubenhet | ||||
| namnlös Universitetet i Cambridge |
Proteinsubenhet, spikeprotein | 2020 | |||
| LUNAR-COV19 Arcturus Therapeutics/Duke University/National University of Singapore |
mRNA-teknik| | Fas I | mitten av 2020 | ||
| namnlös Cobra Biologics/Karolinska Institutet[130] |
DNA-plasmid | 2021 | |||
| namnlös Generex Biotech |
Syntetiska viruspeptider kombinerade med "Ii-nyckel-teknik"[131] | mitten av 2020 | |||
| namnlös Clover Biopharm/Glaxo Smith Kline |
Fragment av spikeprotein | Fas I | |||
| namnlös SK Biosciences/Saskatchewans regering/Korea Centers for Disease Control and Prevention |
Covid-19 antigen-subenheter | september 2020 | |||
| CoroFlu University of Wisconsin–Madison/Flugen/Bharat Biotech |
Icke-replikerande influensavirus | sent 2020 | |||
| namnlös Takis/Evvivax |
DNA | sent 2020 | |||
| AdCOVID Altimmune/University of Alabama |
Icke-replikerande vektor (nässpray) | Fas I | sent 2020 | ||
| namnlös Vaxart/Emergent BioSolutions |
Icke-replikerande vektor (tablett) | Fas I | sent 2020 | ||
| V591 Merck/Institut Pasteur |
Försvagad form av sars-cov-2, med mässlingsvaccin som vektor | Fas I | Försök avbrutna i januari 2021 på grund av dåliga resultat av fas I-försök.[132] | ||
| namnlös Merck |
Fas I | Försök avbrutna i januari 2021 på grund av dåliga resultat av fas I-försök.[133] | |||
| namnlös VBI Vaccines/National Research Council of Canada |
Pan-coronavirus | Försök inleds inte tidigare än i december 2020 | |||
| namnlös Sanofi Pasteur/Translate Bio |
mRNA-teknik[134] | Fas I/II | Försök inleds inte tidigare än i början av 2021 | ||
Se även[redigera | redigera wikitext]
- Europeiska unionens digitala covidintyg
- Richard Bergström, Sveriges vaccinsamordnare
- Covid-19-vaccinering i Sverige
Källor[redigera | redigera wikitext]
- Coronavirus vaccine tracker: how close are we to a vaccine? på The Guardians webbplats den 21 juli 2020
Noter[redigera | redigera wikitext]
- ^ ”The lightning-fast quest for COVID vaccines — and what it means for other diseases”. Nature. 2020-12-18. https://www.nature.com/articles/d41586-020-03626-1. Läst 13 februari 2021.
- ^ Apuzzo, Matt; Kirkpatrick, David D. (1 april 2020). ”Covid-19 Changed How the World Does Science, Together” (på amerikansk engelska). The New York Times. ISSN 0362-4331. https://www.nytimes.com/2020/04/01/world/europe/coronavirus-science-research-cooperation.html. Läst 21 april 2020.
- ^ ”Vaccinutveckling mot coronaviruset går in i nästa fas”. forskning.se. 31 mars 2020. https://www.forskning.se/2020/03/31/vaccinutveckling-mot-coronaviruset-gar-in-i-nasta-fas/. Läst 21 april 2020.
- ^ ”Uni-Virologen beteiligt an Impfstoff-Suche” (på tyska). https://www.giessener-allgemeine.de. 27 mars 2020. https://www.giessener-allgemeine.de/giessen/uni-virologen-beteiligt-impfstoff-suche-13631609.html. Läst 21 april 2020.
- ^ ”Här utvecklas ett svenskt vaccin mot corona”. Forskning & Framsteg. 2 april 2020. https://fof.se/artikel/har-utvecklas-ett-svenskt-vaccin-mot-corona. Läst 21 april 2020.
- ^ [a b] Baden, Lindsey R.; El Sahly, Hana M.; Essink, Brandon; Kotloff, Karen; Frey, Sharon; Novak, Rick (2020-12-30). ”Efficacy and Safety of the mRNA-1273 SARS-CoV-2 Vaccine” (på engelska). New England Journal of Medicine: sid. NEJMoa2035389. doi:. ISSN 0028-4793. http://www.nejm.org/doi/10.1056/NEJMoa2035389. Läst 7 januari 2021.
- ^ [a b] Polack, Fernando P.; Thomas, Stephen J.; Kitchin, Nicholas; Absalon, Judith; Gurtman, Alejandra; Lockhart, Stephen (2020-12-31). ”Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine” (på engelska). New England Journal of Medicine 383 (27): sid. 2603–2615. doi:. ISSN 0028-4793. PMID 33301246. PMC: PMC7745181. http://www.nejm.org/doi/10.1056/NEJMoa2034577. Läst 7 januari 2021.
- ^ [a b] ”First patient receives Pfizer Covid-19 vaccine”. 8 december 2020. https://www.bbc.co.uk/news/uk-55227325. Läst 10 december 2020.
- ^ ”Vaccinationerna i Sverige har inletts — Folkhälsomyndigheten”. www.folkhalsomyndigheten.se. Arkiverad från originalet den 27 december 2020. https://web.archive.org/web/20201227105629/https://www.folkhalsomyndigheten.se/nyheter-och-press/nyhetsarkiv/2020/december/vaccinationerna-i-sverige-har-inletts/. Läst 27 december 2020.
- ^ Beaumont, Peter (18 november 2020). ”Covid-19 vaccine: who are countries prioritising for first doses?” (på brittisk engelska). The Guardian. ISSN 0261-3077. https://www.theguardian.com/world/2020/nov/18/covid-19-vaccine-who-are-countries-prioritising-for-first-doses. Läst 4 januari 2021.
- ^ ”Coronavirus (COVID-19) Vaccinations - Statistics and Research”. Our World in Data. https://ourworldindata.org/covid-vaccinations. Läst 13 januari 2021.
- ^ Mullard, Asher (2020-11-30). ”How COVID vaccines are being divvied up around the world” (på engelska). Nature. doi:. https://www.nature.com/articles/d41586-020-03370-6. Läst 4 januari 2021.
- ^ So, Anthony D.; Woo, Joshua (2020-12-15). ”Reserving coronavirus disease 2019 vaccines for global access: cross sectional analysis” (på engelska). BMJ 371. doi:. ISSN 1756-1833. PMID 33323376. PMC: PMC7735431. https://www.bmj.com/content/371/bmj.m4750. Läst 4 januari 2021.
- ^ [a b] Richard Bergström i Svenskar kan bli testpiloter när vaccinstudier går in slutfasen i Dagens Nyheter den 21 juli, sidan 06]
- ^ Covid-19 Vaccine & Therapeutics Tracker på www.biorender.com, läst den 20 juli 2020
- ^ Draft landscape of COVID-19 candidate vaccines – Overview med länk till detaljer i pdf-format på WHO:s webbplats,läst den 8 december 2020
- ^ ”G20 launches initiative for health tools needed to combat the coronavirus”. https://www.theglobeandmail.com/world/article-g20-launches-initiative-for-health-tools-needed-to-combat-the-2/. Läst 4 januari 2021.
- ^ ”WHO Director-General's opening remarks at the launch of the Access to COVID-19 Tools Accelerator” (på engelska). www.who.int. https://www.who.int/director-general/speeches/detail/who-director-general-s-opening-remarks-at-the-launch-of-the-access-to-covid-19-tools-accelerator. Läst 4 januari 2021.
- ^ Rauhala, Emily; Abutaleb, Yasmeen. ”U.S. says it won’t join WHO-linked effort to develop, distribute coronavirus vaccine” (på amerikansk engelska). Washington Post. ISSN 0190-8286. https://www.washingtonpost.com/world/coronavirus-vaccine-trump/2020/09/01/b44b42be-e965-11ea-bf44-0d31c85838a5_story.html. Läst 4 januari 2021.
- ^ ”ACT-Accelerator FAQ” (på engelska). www.who.int. https://www.who.int/initiatives/act-accelerator/faq. Läst 4 januari 2021.
- ^ ”Our portfolio” (på amerikansk engelska). CEPI. https://cepi.net/research_dev/our-portfolio/. Läst 4 januari 2021.
- ^ ”Global equitable access to COVID-19 vaccines estimated to generate economic benefits of at least US$ 153 billion in 2020–21, and US$ 466 billion by 2025, in 10 major economies, according to new report by the Eurasia Group” (på engelska). www.who.int. https://www.who.int/news/item/03-12-2020-global-access-to-covid-19-vaccines-estimated-to-generate-economic-benefits-of-at-least-153-billion-in-2020-21. Läst 4 januari 2021.
- ^ ”EU spearheads $8 billion virus fundraiser” (på amerikansk engelska). finance.yahoo.com. https://finance.yahoo.com/news/eu-hosts-virus-telethon-seeking-first-7-5-003500556.html. Läst 4 januari 2021.
- ^ News, A. B. C.. ”Bill and Melinda Gates Foundation announces $250 million COVID vaccine commitment” (på engelska). ABC News. https://abcnews.go.com/Technology/bill-melinda-gates-foundation-announces-250-million-covid/story?id=74651890. Läst 4 januari 2021.
- ^ ”Bill and Melinda Gates call for collaboration innovation to deliver COVID 19 breakthroughs” (på engelska). www.gatesfoundation.org. 1 januari 2001. https://www.gatesfoundation.org/Media-Center/Press-Releases/2020/12/Bill-and-Melinda-Gates-call-for-collaboration-innovation-to-deliver-COVID-19-breakthroughs. Läst 4 januari 2021.
- ^ ”Novel Coronavirus COVID-19 – GloPID-R”. www.glopid-r.org. Arkiverad från originalet den 2 maj 2020. https://web.archive.org/web/20200502035337/https://www.glopid-r.org/our-work/novel-coronavirus-covid-19/. Läst 4 januari 2021.
- ^ ”Third-Generation Vaccines Take Center Stage in Battle Against COVID-19”. Lexology. 30 november 2020. https://www.lexology.com/library/detail.aspx?g=04bdfa93-c8ea-4654-a5f1-c659fc4769c8. Läst 28 december 2020.
- ^ ”‘Nocebo effect’: two-thirds of Covid jab reactions not caused by vaccine, study suggests” (på engelska). the Guardian. 18 januari 2022. https://www.theguardian.com/science/2022/jan/18/nocebo-effect-two-thirds-of-covid-jab-reactions-not-caused-by-vaccine-study-suggests. Läst 22 januari 2022.
- ^ ”The nocebo effect explained—new study attributes COVID-19 vaccine symptoms to phenomenon” (på engelska). Newsweek. 20 januari 2022. https://www.newsweek.com/coronavirus-nocebo-effect-definition-new-study-covid-19-vaccine-symptoms-1671115. Läst 22 januari 2022.
- ^ Seasonal coronavirus protective immunity is short-lasting Nature 14 september 2020
- ^ Professor: Vaccinet innebär inte att vi kan slappna av Sveriges Television 28 december 2020
- ^ A Guide to Emerging SARS-CoV-2 Variants The Scientist 26 januari 2021
- ^ Will Delaying Vaccine Doses Cause a Coronavirus Escape Mutant? The Scientist 04 februari 2021
- ^ Vaccines Versus the Mutants The Scientist 08 februari 2021
- ^ Could new COVID variants undermine vaccines? Labs scramble to find out Nature 07 januari 2021
- ^ AstraZeneca plans booster jab for new variants, as mutation fears grow CGTN 12 februari 2021
- ^ Moderna Developing Booster Shot for New Virus Variant B.1.351 The Scientist 25 januari 2021
- ^ EMA preparing guidance to tackle COVID-19 variants EMA 10 februari 2021
- ^ ”COVID-19 vaccine development pipeline (Refresh URL to update)”. Vaccine Centre, London School of Hygiene and Tropical Medicine. 11 maj 2020. https://vac-lshtm.shinyapps.io/ncov_vaccine_landscape/.
- ^ ”COVID-19 vaccine tracker (Choose vaccines tab; updated 2-3x/week)”. Milken Institute. 12 maj 2020. https://docs.google.com/spreadsheets/d/16DbPhF9OD0MHHtCR12of6yUcfiRzP_-XGkynEbnipds/edit#gid=1804775590.
- ^ Coronavirus Vaccine Tracker på New York Times webbplats den 20 juli 2020
- ^ [a b] [1], Covid vaccine landscape på Vaccine Centres, London School of Hygiene and Tropical Medicines webbplats, den 21 december 2020
- ^ Oxford/AstraZeneca Covid vaccine has 70% efficacy, full trial data shows i The Guardian den 8 december
- ^ Adam Finn: Ten reasons we got Covid-19 vaccines so quickly without 'cutting corners' i The Guardian den 26 december 2020
- ^ Covid: What do we know about China's coronavirus vaccines? på BBC:s webbplats den 30 december 2020
- ^ ”COVID-19 Vaccine Moderna dispersion for injection mRNA Vaccine (nucleoside modified)”. EMA. Arkiverad från originalet den 6 mars 2021. https://web.archive.org/web/20210306012007/https://www.ema.europa.eu/en/documents/product-information/covid-19-vaccine-moderna-epar-product-information_en.pdf. Läst 6 mars 2021.
- ^ ”COVID-19 Vaccine AstraZeneca suspension for injection (ChAdOx1-S [recombinant)”]. EMA. https://www.ema.europa.eu/en/documents/product-information/covid-19-vaccine-astrazeneca-epar-product-information_en.pdf. Läst 6 mars 2021.
- ^ ”Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK” (på engelska). The Lancet. 8 december 2020. https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(20)32661-1/fulltext. Läst 4 mars 2021.
- ^ ”Comirnaty, INN-COVID-19 mRNA Vaccine (nucleoside-modified)”. EMA. https://www.ema.europa.eu/en/documents/product-information/comirnaty-epar-product-information_en.pdf. Läst 4 mars 2021.
- ^ [a b c] [https://www.fda.gov/media/144413/download ”EMERGENCY USE AUTHORIZATION (EUA) OF THE PFIZER-BIONTECH COVID-19 VACCINE TO PREVENT CORONAVIRUS DISEASE 2019 (COVID-19)”]. FDA. https://www.fda.gov/media/144413/download. Läst 6 mars 2021.
- ^ [a b] ”EMA recommends COVID-19 Vaccine Janssen for authorisation in the EU”. EMA. https://www.ema.europa.eu/en/news/ema-recommends-covid-19-vaccine-janssen-authorisation-eu. Läst 11 mars 2021.
- ^ ”Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia” (på engelska). The Lancet. 2 februari 2021. https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(21)00234-8/fulltext. Läst 4 mars 2021.
- ^ China Covid vaccine reports mixed results — what does that mean for the pandemic? på www.nature.com den 15 januari 2021
- ^ [a b] Covaxin and Covishield: What we know about India's Covid vaccines på www.bbc.com den 22 januari 2021
- ^ ”Draft landscape and tracker of COVID-19 candidate vaccines” (på engelska). www.who.int. https://www.who.int/publications/m/item/draft-landscape-of-covid-19-candidate-vaccines. Läst 30 januari 2021.
- ^ EMA starts rolling review of the Sputnik V COVID-19 vaccine den 04 mars 2021
- ^ ”UK medicines regulator gives approval for first UK COVID-19 vaccine”. GOV.UK. 2 december 2020. https://www.gov.uk/government/news/uk-medicines-regulator-gives-approval-for-first-uk-covid-19-vaccine. Läst 10 december 2020.
- ^ ”Bahrain becomes second nation to grant emergency use for Pfizer, BioNTech vaccine” (på engelska). 5 december 2020. https://www.9news.com.au/world/coronavirus-news-bahrain-grants-emergency-use-for-pfizer-biontech-vaccine/7b3a0765-b872-4786-960f-b5bcb2aacef6. Läst 10 december 2020.
- ^ Kelly Grant (9 december 2020). ”Health Canada approves Pfizer's COVID-19 vaccine. Here's what you need to know about it”. The Globe and Mail. https://www.theglobeandmail.com/canada/article-health-canada-approves-pfizer-vaccine-heres-what-you-need-to-know/. Läst 10 december 2020.
- ^ Pfizer-BioNTech COVID-19 Vaccine (tozinameran) på Health Canadas webbplats den 9 december
- ^ First vaccine shipments will arrive in states on Monday på www.politico-com den 12 december 2020
- ^ [a b] ”EU-kommissionen godkänner det första säkra och verksamma vaccinet mot covid-19”. EU-kommissionen. 21 december 2020. https://ec.europa.eu/commission/presscorner/detail/sv/ip_20_2466h. Läst 26 december 2020.
- ^ [a b] New York Times den 18 december 2020
- ^ [a b] ”EU-kommissionen godkänner det andra säkra och verksamma vaccinet mot covid-19”. Europeiska Kommissionen. https://ec.europa.eu/commission/presscorner/detail/sv/IP_21_3. Läst 6 januari 2021.
- ^ Covid-19: Oxford-AstraZeneca coronavirus vaccine approved for use in UK på BBC:s webbplats den 30 december 2020
- ^ [a b c] India approves two vaccines as it prepares for massive immunization campaign i Washington Post den 3 januari 2021
- ^ [a b] ”European Commission authorises third safe and effective vaccine against COVID-192021”. Europeiska Kommissionen. https://ec.europa.eu/commission/presscorner/detail/sv/ip_21_306. Läst 29 januari 2021.
- ^ [a b] FDA Issues Emergency Use Authorization for Third COVID-19 Vaccine på www.fda.gov den 28 februari 2021
- ^ [a b] ”EU-kommissionen godkänner det fjärde säkra och verksamma vaccinet mot covid-19”. Europeiska Kommissionen. https://ec.europa.eu/commission/presscorner/detail/sv/ip_21_1085. Läst 11 mars 2021.
- ^ China approves Sinopharm Covid-19 vaccine for general use i The Guardian den 31 december 2020
- ^ Bahrain approves registration for Sinopharm COVID-19 vaccine på www.reuters.com den 13 december 2020
- ^ Indonesia approves China’s CoronaVac for emergency use Decision based on results of country's Phase III trials that put estimated vaccine efficacy at 65.3%, says official på www.aa.com den 11 januari 2021
- ^ China approves Sinovac Biotech COVID-19 vaccine for general public use på www.reuters.com den 6 februari
- ^ [a b] France's Sanofi and Britain's GSK said Friday their Covid-19 vaccines will not be ready until the end of 2021, after interim results showed a low immune response in older adults. på www.france24.com den 11 december 2020
- ^ EMA starts rolling review of mRNA COVID-19 vaccine by Moderna Biotech Spain, S.L. den 16 november 2020
- ^ EMA receives application for conditional marketing authorisation of Moderna COVID-19 vaccine den 1 december 2020
- ^ [a b] ”EMA recommends COVID-19 Vaccine Moderna for authorisation in the EU”. EMA. https://www.ema.europa.eu/en/news/ema-recommends-covid-19-vaccine-moderna-authorisation-eu. Läst 6 januari 2021.
- ^ EMA starts first rolling review of a COVID-19 vaccine in the EU den 1 oktober 2020
- ^ EMA receives application for conditional marketing authorisation of COVID-19 Vaccine AstraZeneca den 29 januari 2021
- ^ ”EMA recommends COVID-19 Vaccine AstraZeneca for authorisation in the EU”. EMA. https://www.ema.europa.eu/en/news/ema-recommends-covid-19-vaccine-astrazeneca-authorisation-eu. Läst 29 januari 2021.
- ^ AstraZenecas vaccin rekommenderas för alla över 18 år på Folkhälsomyndighetens webbplats Arkiverad 7 mars 2021 hämtat från the Wayback Machine. den 4 mars 2021]
- ^ EMA starts second rolling review of a COVID-19 vaccine den 6 oktober 2020
- ^ EMA receives application for conditional marketing authorisation of COVID-19 mRNA vaccine BNT162b2 den 1 december 2020
- ^ ”EMA recommends first COVID-19 vaccine for authorisation in the EU”. EMA. https://www.ema.europa.eu/en/news/ema-recommends-first-covid-19-vaccine-authorisation-eu. Läst 21 december 2020.
- ^ ”Comirnaty - vaccin mot covid-19 | Läkemedelsverket / Swedish Medical Products Agency”. www.lakemedelsverket.se. https://www.lakemedelsverket.se/sv/coronavirus/coronavaccin/comirnaty---vaccin-mot-covid-19. Läst 4 januari 2021.
- ^ EMA starts rolling review of Janssen’s COVID-19 vaccine Ad26.COV2.S den 1 december 2020
- ^ EMA receives application for conditional marketing authorisation of COVID-19 Vaccine Janssen den 16 februari 2021
- ^ ”COVID-19 Vaccine Janssen suspension for injection vaccine (Ad26.COV2-S recombinant)”. EMA. Arkiverad från originalet den 11 mars 2021. https://web.archive.org/web/20210311195116/https://www.ema.europa.eu/en/documents/product-information/covid-19-vaccine-janssen-epar-product-information_en.pdf. Läst 11 mars 2021.
- ^ EMA starts rolling review of Novavax’s COVID-19 vaccine (NVX-CoV2373) den 2 februari 2021
- ^ EMA receives application for conditional marketing authorisation of Novavax’s COVID-19 vaccine, Nuvaxovid den 17 november 2021
- ^ EMA recommends Nuvaxovid for authorisation in the EU den 20 december 2021
- ^ EU-kommissionen godkänner det femte säkra och verksamma vaccinet mot covid-19 den 20 december 2021
- ^ EMA starts rolling review of the Sputnik V COVID-19 vaccine den 04 mars 2021
- ^ EMA starts rolling review of COVID-19 Vaccine (Vero Cell) Inactivated den 05 april 2021
- ^ EMA starts rolling review of COVID-19 vaccine Vidprevtyn den 20 juli 2021
- ^ EMA starts rolling review of Valneva’s COVID-19 vaccine (VLA2001) den 02 december 2021
- ^ Pfizer-BioNTech COVID-19 Vaccine på Food and Drug Administrations webbplats den 12 december 2020
- ^ Science & Tech Spotlight Covid-19 vacine development, US Government Accountability Offices webbplats, maj 2020
- ^ Draft landscape of Covid-19 vaccines på Världshälsoorganisationens webbplats, läst den 8 december 2020]
- ^ Rees, Victoria (1 juli 2020). ”First COVID-19 vaccine given green light for Phase I trial in China”. European Pharmaceutical Review. https://www.europeanpharmaceuticalreview.com/news/122608/first-covid-19-vaccine-given-green-light-for-phase-i-trial-in-china/. Godkänd för Fas I i Kina i slutet av juni 2020.
- ^ Chinese vaccines slower than Pfizer in WHO validation, but ‘intl orders unaffected’ på www.globaltimes.cn den 8 januari 2021
- ^ COVID-19 vaccine AZD1222 showed robust immune responses in all participants in Phase I/II trial, pressmeddelande från Astra Zeneca den 20 juli 2020, efter publicering av tidiga resultat i The Lancet samma dag
- ^ Pfizer, BioNTech nab fast track tag, prep for major phase 3 COVID-19 vax test this month på www.fiercebiotech.com den 13 juli 2020
- ^ Positiva resultat från fas I–II redovisade i juli Pfizer and BioNTech Announce Early Positive Update from German Phase 1/2 COVID-19 Vaccine Study, Including First T Cell Response Data, pressmeddelande från Pfizer och Biontech på www.globenewswire.com den 20 juli 2020
- ^ [a b c] Sinovac collaboration could see COVID-19 vaccine ready by early 2021, Bio Farma claims i The Jakarta Post den 17 juli 2020
- ^ Indonesia approves China’s CoronaVac for emergency use Decision based on results of country's Phase III trials that put estimated vaccine efficacy at 65.3%, says official på www.aa.com den 11 januari 2021
- ^ China approves Sinovac Biotech COVID-19 vaccine for general public use på www.reuters.com den 6 februari
- ^ Inovio Announces Positive Interim Phase 1 Data For INO-4800 Vaccine for COVID-19 på Inovios webbplats
- ^ [a b] Moderna finalises protocol for Phase 3 Covid-19 vaccine trial på www.clinicaltrialsarena.com den 12 juni 2020
- ^ An mRNA Vaccine against SARS-CoV-2 — Preliminary Report i New England Journal of Medicine den 14 juli 2020
- ^ [a b] Coronavirus vaccine from Chinas's Sinopharm is 86% effective, UAE officials say i Washington Post den 9 december 2020
- ^ Om Covaxin på Bharat Biotechs webbplats
- ^ NVX-CoV2373 SARS-CoV-2 Vaccine på Novavax webbplats den 7 juli 2020
- ^ Novavax launches pivotal U.S. trial of dark horse COVID-19 vaccine after manufacturing delays på www.sciencemag.org deb 28 december 2020
- ^ ”Medico begins Phase 1 clinical trials for its Covid-19 vaccine candidate på Medicos webbplats den 14 juli 2020”. Arkiverad från originalet den 22 juli 2020. https://web.archive.org/web/20200722102219/https://www.medicago.com/en/newsroom/medicago-begins-phase-i-clinical-trials-for-its-covid-19-vaccine-candidate/. Läst 21 juli 2020.
- ^ Coronavirus vaccine: Canada-based Medicago develops plant-based vaccine, starts phase I trials i Times of India den 16 juli 2020
- ^ CureVac Receives Regulatory Approval from German and Belgian Authorities to Initiate Phase 1 Clinical Trial of its SARS-CoV-2 Vaccine Candidate på CureVacs webbplats den 17 juni 2020
- ^ Vaccine candidate against SARS-CoV-2 being tested på Science Daily den 3 april 2020
- ^ EMA ends rolling review of CVnCoV COVID-19 vaccine following withdrawal by CureVac AG på www.ema.europa.eu 12 oktober 2021
- ^ Sputnik V:s webbplats
- ^ Covid-19 vaccine tracker, July 30: Russian vaccine to be ready by August 12 i Indian Express den 31 juli 2020
- ^ Dagens Nyheter den 12 augusti 2020, sidan 15
- ^ Registreringsbevis
- ^ Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia på www.thelancet.com 02 februari 2021
- ^ First volunteers receive Imperial COVID-19 vaccine på Imperial Colleges webbplats den 23 juni 2020
- ^ Self-amplifying mRNA (SAM) Vaccine Platform på www.creative-biolabs.com, läst den 21 juli 2020
- ^ Clinicaltrials.gov den 9 mars 2020
- ^ Clinicaltrials.gov den 19 mars 2020
- ^ UPMC and University of Pittsburgh School of Medicine Scientists Announce Potential Vaccine, på University of Pittsburgs webbplats, odaterat, läst den 20 juli 2020
- ^ Cobra Biologics and the Karolinska Institutet collaborate to develop COVID-19 vaccine på Cobra Biologics webbplats den 30 mars 2020
- ^ Generex Provides Summary of Ii-Key Hybrid Vaccine Platform på www.businesswire.com den 7 augusti 2017
- ^ Merck abandons bid to develop Covid-19 vaccine i Financial Times den 25 januari 2021
- ^ Merck abandons bid to develop Covid-19 vaccine i Financial Times den 25 januari 2021
- ^ Sanofi and Translate Bio mRNA COVID-19 vaccine candidate induced high antibody levels in preclinical studies på www.sanofi.com Arkiverad 27 januari 2021 hämtat från the Wayback Machine., läst den 28 januari 2021
Externa länkar[redigera | redigera wikitext]
 Wikimedia Commons har media som rör Covid-19-vaccin.
Wikimedia Commons har media som rör Covid-19-vaccin.- Uppdaterad information från Folkhälsomyndigheten om covid-19
- Uppdaterad information från WHO om vaccin mot covid-19
| ||||||||||||||||
| ||||||||||||||||||||||


