Glutenintolerans
| Celiaki | |
| Latin: coeliacia | |
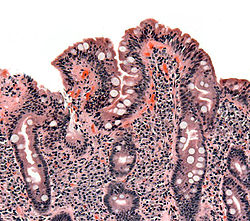 Biopsi av tunntarmen som visar tecken på celiaki; avtrubbade villi, hyperplasi i kryptorna med infiltration av lymfocyter. | |
| Klassifikation och externa resurser | |
|---|---|
| ICD-10 | K90.0 |
| ICD-9 | 579.0 |
| OMIM | 212750 |
| DiseasesDB | 2922 |
| Medlineplus | 000233 |
| eMedicine | med/308 ped/2146 |
| MeSH | svensk engelsk |
Celiaki (även känt som glutenintolerans, trots att det är en immunologisk överkänslighet) är en autoimmun sjukdom där det finns antikroppar mot ett i gluten förekommande glykoprotein. Sjukdomen orsakar skador på tunntarmens slemhinna.
Beroende på vilket sädesslag det handlar om är glykoproteinet antingen gliadin (vete), sekalin (råg) eller hordein (korn). Antikropparna som bildas är mot gliadiner, men både sekaliner och hordeiner är så lika att de också sätter igång immunförsvaret. Avenin, prolaminet i havre, verkar inte vara lika benäget att skapa ett immunsvar.
Celiaki ska inte förväxlas med spannmålsallergi eller det vanligen förekommande uttrycket glutenallergi, som är en tidigare benämning på spannmålsallergi.
Historik[redigera | redigera wikitext]
Namnet celiaki och symptombeskrivningen finns redan beskrivet under det första århundradet efter Kristus av den grekiska läkaren Aretaeus av Kappadokien. Han döpte det till "koiliakos" efter grekiskans "koelia" (buk). Hans beskrivning av sjukdomen löd: "Om magen inte kan bibehålla mat, den passerar osmält och rå och inget tas upp av kroppen så kallar vi sådana människor celiaker."
På 1800-talet publicerade Mathew Baillie sin avhandling om en kronisk diarrésjukdom hos vuxna som innebar näringsbrist. Ofta kännetecknad av en gas-svullen buk. Han föreslog att dessa människor skulle gå igenom en kostbehandling, då hans observationer hade visat att patienterna blev friskare om de bytte till en kost som i princip enbart bestod av ris.
Baillies observationer gick dock förbi i princip obemärkta och forskningen inom celiaki tog sitt första stora språng 75 år senare i England. Samuel Gee, en då ledande person inom pediatrisk vård höll ett föredrag för medicinstudenter om "affektiv celiaki". Precis som Baillie menade Gee att patienterna enbart skulle kunna bli friska genom en kostförändring. Han hade bland annat gjort observationer på ett barn som led svårt av sjukdomen, men som blev friskt under musselsäsongen då barnet bytte ut stora delar av sin kost mot musslor. När musselsäsongen var över och barnet återgick till sin vanliga kost återkom alla sjukdomssymptom. Det här är historiens första skriftliga dokumentation av en patient som blev friskare av att undvika gluten och blev sjuk på nytt efter att man introducerade det igen.
Trots Baillies och Gees observationer samt regelbundna obduktioner (dödsrisken var hög) gick det flera decennier innan läkarvetenskapen identifierat att det var just gluten som var skälet till att patienterna blev sämre.
Under 1920-talet uppkom den första behandlingen för folk med celiaki: banandieten. Sidney Haas publicerade en studie som rörde tio barn med celiaki. Åtta av dem hade fått byta ut bröd, kex och potatis mot bananer, medan två av dem fick fortsätta äta som vanligt. De åtta som fick förändrad kost blev "kliniskt friska" medan de två barn som fick oförändrad kost dog. Denna studie bemöttes med en popularitet utan tidigare motstycke, och i flera decennier tillämpades dess idéer av vuxna och barn med celiaki. Den förhindrade förmodligen många dödsfall med tanke på att den exkluderade kost som innehöll spannmål.
Haas var väldigt stolt över sin upptäckt och var övertygad om att stärkelse var den enda sanna boven i dramat trots andra väl utförda studier som visade på annat. Läkaren Willem-Karel Dicke observerade att barn som led av celiaki i Nederländerna blev betydligt friskare under andra världskriget när det rådde stor brist på vete, medan de snabbt insjunknade på nytt när de allierades plan släppte ner brödransoner till det nederländska folket. År 1950 skrev han en avhandling som gick ut på att gluten i vete var det som gjorde människor med celiaki sjuka, och inte stärkelse som tidigare påståtts.
Det första stora genombrottet rörande skadan på tunntarmen upptäcktes av Margot Shiner under mitten av 1950-talet. Hon hade uppfunnit ett nytt sätt att genomföra obduktioner, vilket till slut gjorde det möjligt att göra jämförelser mellan skador på tunntarmen hos folk med celiaki och friska människor. Kort därefter uppfanns ett smidigare sätt att utföra biopsi av en överstelöjtnant Crosby och man kunde för första gången jämföra levande patienter med celiaki med tidigare dödsfall.
Fram till 1970-talet fanns det inga fastställda diagnostiska kriterier för celiaki. Då infördes systemet att patienten först skulle genomgå en biopsi för att kontrollera slemhinnan, därefter sluta äta gluten och genomgå ytterligare en biopsi, och sedan en till, efter att tarmen hade provocerats med högglutenhaltig kost.[1] Det här diagnoskravet ställdes av European Society for Pediatric Gastroenterology, ESPGHAN och var standard i de tjugo kommande åren.
Tyvärr ignorerade ESPGHAN avhandlingar av Berger några år tidigare, 1964, som dokumenterade gliadinantikroppar i blodet hos barn med celiaki. Sju år senare tog forskningen ett steg framåt, men först långt senare accepterades blodprov som ett led i diagnosen av celiaki.
Under 1980-talet började allt fler forskare se likheter mellan celiaki och andra autoimmuna sjukdomar, bland annat typ 1-diabetes. Senare under 1980-talet uppfanns en ny typ av procedur inom biopsi som gjorde det möjligt att ställa diagnos på tunntarmen med hjälp av enbart en biopsi i stället för tre. De nya riktlinjerna för diagnos publicerades 1990 av ESPGHAN och är de kriterier som gäller än idag.
Kort därefter blev det internationellt accepterat att celiaki är en autoimmun sjukdom och inte bara en tarmsjukdom som tidigare förmodat.
Sedan 2012 är det i vissa fall möjligt att ställa diagnos utan biopsi. Då krävs tillräckligt höga värden av glutenantikroppar i blodet vid minst två separata tillfällen. Det nya diagnossättet är 95 % säkert.
Symptom[redigera | redigera wikitext]
Symptomen är kopplade till malabsorption i tunntarmen. När immunsvaret reagerar mot en prolamin (exempelvis gliadin) i en överkänslig person sätts en inflammation igång i tarmen som förstör dess villi och därmed drastiskt minskar den yta som finns tillgänglig för upptag av alla näringsämnen. En person med celiaki kan uppvisa bristsymptom då upptag av alla vitaminer och även protein, fett och glukos är hämmat.
Det finns dock vissa tecken som ska föranleda misstanke om celiaki:
- viktminskning (hos barn frånvaro av viktuppgång / barnet följer inte tillväxtkurvan)
- diarré/stor avföringsvolym/gasbesvär. Steatorré (fett i faeces) är ett tecken på malabsorption av fett.
- trötthet/svaghet
- infertilitet
- förstoppning
- vitamin-, mineral- eller blodbrist
Patienter med celiaki löper ökad risk för bland annat diabetes, sköldkörtelsjukdom, och osteoporos (benbrott, frakturer). De vanligaste dödsorsakerna bland patienter med celiaki är cancer och hjärtkärlsjukdom [2], vilket också gäller för normalbefolkningen [3].
Diagnos[redigera | redigera wikitext]
De blodprov som tas för att se om patienten lider av celiaki är vanligen antikroppar mot gliadin (AGA) i kombination med antingen anti-endomysiumantikroppar (EmA) eller anti-transglutaminasantikroppar (tTG). Ett vävnadsprov (biopsi) från tunntarmen tages så gott som alltid. Vävnadsprovets histologiska bild är definitivt avgörande för diagnosen celiaki.
Tunntarmsbiopsin bedöms utefter olika skalor till exempel Alexandergradering (från I-IV), KVAST-klassifikation eller Marsh-skalan. Ändringar i bedömningen utförda i inte alltför avlägsen tid gör att en del patienter som tror sig vara utredda för och inte lidande av celiaki nu skulle diagnostiseras med celiaki om testet gjordes igen.
Sjukdomsförlopp[redigera | redigera wikitext]
Det finns rapporter om att sjukdomen hos unga har läkt, men om man diagnostiseras som äldre är risken stor att det är ett livslångt tillstånd. De som tillfrisknat från celiaki har sannolikt fått en felaktig diagnos från början, då celiaki är livslångt. Om en person med celiaki ändå äter gluten kommer en inflammation av tunntarmen följa och metalloproteinaser (MMP) utsläppta av immunceller kommer leda till villusatrofi och minskad absorptionsyta.
Orsaker[redigera | redigera wikitext]
Celiaki är inte nödvändigtvis medfött, utan kan förvärvas även senare i livet. Sjukdomen är dubbelt så vanlig hos kvinnor som hos män.[1] I Sverige beräknas cirka 2 procent av befolkningen som helhet vara drabbad,[4] medan siffran är 3 procent för de födda mellan 1984 och 1996.[1] Hur sjukdomen uppkommer är inte säkerställt, men en tysk forskargrupp hittade 1997 en viktig pusselbit[5] när de identifierade transglutaminas som ett antigen i sjukdomen. Detta, och att 95% av de med celiaki har haplotypen HLA DQ2/DQ8, har dock gett många ledtrådar.
Gluten består av de två peptiderna gliadin och glutenin som båda är immunogena och resistenta mot nedbrytning i tarmen. Av okänd anledning kan dessa två peptider tränga igenom tarmens slemhinna i situationer där slemhinnan försvagats av exempelvis en tarminfektion. Därefter kommer transglutaminaser katalysera en deamidering av peptiderna vilket bildar starkt immunogena epitoper. I genetiskt betingade individer alstrar immunsystemet en reaktion mot epitoperna och även mot transglutaminaset. Följden blir inflammation och rekrytering av leukocyter till tarmsystemet med villusatrofi som följd.
Behandling[redigera | redigera wikitext]
Med glutenfri kost blir tarmen långsamt helt normal, i den mening att man är frisk, den glutenfria dieten måste fortfarande hållas. Sannolikheten att celiaki i sig försvinner är väldigt liten. Exempel på bra glutenfria kolhydrater är potatis, ris, hirs, majs, bovete, quinoa och amaranth. Ett bra bröd kan bakas av bovete, hirs och linfrö. I livsmedelsbutikerna har sortimentet ökat de senaste åren vad gäller sortimentet av glutenfria matvaror. Idag finns det glutenfria produkter i de flesta livsmedelsaffärer och utbudet ökar för varje år vilket underlättar för personer drabbade av celiaki. Apoteket tillhandahåller också sådana varor.
Se även[redigera | redigera wikitext]
Referenser[redigera | redigera wikitext]
- ^ [a b c] Browaldh, Lars; överläkare; Barngastroenterologi, Sektionen För; barnsjukhuset, Sachsska; Södersjukhuset; ström. ”Celiaki är en vanlig sjukdom som är lätt att missa”. lakartidningen.se. Arkiverad från originalet den 10 april 2019. https://web.archive.org/web/20190410084759/http://www.lakartidningen.se/Klinik-och-vetenskap/Klinisk-oversikt/2014/03/Celiaki-ar-en-vanlig-sjukdom-som-ar-latt-att-missa/. Läst 10 april 2019.
- ^ Ludvigsson JF, Montgomery SM, Ekbom A, Brandt L, Granath F (23 april 2009). ”Small-intestinal histopathology and mortality risk in celiac disease”. JAMA "302" (11): ss. 1171–8. doi:. PMID 19755695.
- ^ ”Dödsorsaker 2009 (Socialstyrelsen)”. Arkiverad från originalet den 19 december 2014. https://web.archive.org/web/20141219112649/http://www.socialstyrelsen.se/Lists/Artikelkatalog/Attachments/18270/2011-3-22.pdf. Läst 19 december 2014.
- ^ ”Livsmedelsverket”. www.livsmedelsverket.se. Arkiverad från originalet den 21 mars 2019. https://web.archive.org/web/20190321194649/https://www.livsmedelsverket.se/matvanor-halsa--miljo/sjukdomar-allergier-och-halsa/allergi-och-overkanslighet/gluten. Läst 10 april 2019.
- ^ Identification of tissue transglutaminas as the autoantigen of celiac disease. Nat Med 1997;3:797-801
Externa länkar[redigera | redigera wikitext]
- ”Glutenintolerans och spannmålsallergi”. Livsmedelsverket. 3 oktober 2017. Arkiverad från originalet den 27 oktober 2017. https://web.archive.org/web/20171027130013/https://www.livsmedelsverket.se/matvanor-halsa--miljo/sjukdomar-allergier-och-halsa/allergi-och-overkanslighet/gluten. Läst 27 oktober 2017.
- ”Glutenintolerans”. 1177 Vårdguiden. 9 mars 2016. https://www.1177.se/sjukdomar--besvar/allergier-och-overkanslighet/celiaki/celiaki/. Läst 27 oktober 2017.
- Svenska Celiakiförbundets webbplats
| |||||||||||
